CARBONO.pptx
- 1. CARBONO
- 2. EL CARBONO ES UN ELEMENTO QUÍMICO PERTENECIENTE AL GRUPO 14 DE LA TABLA PERIÓDICA DE LOS ELEMENTOS, CON NÚMERO ATÓMICO 6, Y CUYO SÍMBOLO ES C. ES SÓLIDO A TEMPERATURA AMBIENTE Y PUEDE ENCONTRARSE EN LA NATURALEZA EN DOS FORMAS ALOTRÓPICAS: CARBONO AMORFO (GRAFITO) Y CARBONO CRISTALINO (DIAMANTE).
- 3. HIBRIDACIONES DEL CARBONO LA HIBRIDACIÓN CONSISTE EN UNA MEZCLA DE ORBITALES PUROS EN UN ESTADO EXCITADO PARA FORMAR ORBITALES HÍBRIDOS EQUIVALENTES CON ORIENTACIONES DETERMINADAS EN EL ESPACIO. MEDIANTE LA HIBRIDACIÓN, ADEMÁS DE HACER POSIBLE LA TETRAVALENCIA DEL CARBONO, PERMITIENDO FORMAR ORBITALES MÁS ESTABLES, Y ÉSTOS A SU VEZ, ENLACES MÁS
- 4. HIBRIDACIÓN SP3 O TETRAÉDRICA PARA LOS COMPUESTOS EN LOS CUALES EL CARBONO PRESENTA ENLACES SIMPLES, HIDROCARBUROS SATURADOS O ALCANOS, SE HA PODIDO COMPROBAR QUE LOS CUATRO ENLACES SON IGUALES Y QUE ESTÁN DISPUESTOS DE FORMA QUE EL NÚCLEO DEL ÁTOMO DE CARBONO OCUPA EL CENTRO DE UN TETRAEDRO REGULAR Y LOS ENLACES FORMAN ÁNGULOS IGUALES DE 109º 28' DIRIGIDOS HACIA LOS VÉRTICES DE UN TETRAEDRO. ESTA CONFIGURACIÓN SE EXPLICA SI SE CONSIDERA QUE LOS TRES ORBITALES 2P Y EL ORBITAL 2S SE HIBRIDAN PARA FORMAR CUATRO ORBITALES HÍBRIDOS SP3.
- 7. REACCIONES DEL CARBONO •TIPO DE REACCIONES ORGANICAS •Una reacción química se puede definir como un proceso de interacción entre especies químicas y en el que, como consecuencia de la ruptura y formación de enlaces, se origina una nueva entidad química. A continuación, se indican diferentes métodos de clasificación de la reacciones más usuales en Química Orgánica.
- 11. Fórmula molecular •La fórmula molecular expresa el número real de átomos que forman una molécula a diferencia de la fórmula química que es la representación convencional de los elementos que forman una molécula o compuesto químico. Una fórmula molecular se compone de símbolos y subíndices numéricos; los símbolos corresponden a los elementos que forman el compuesto químico representado y los subíndices son la cantidad de átomos presentes de cada elemento en el compuesto.1 Así, por ejemplo, una molécula de ácido sulfúrico, descrita por la fórmula molecular H2SO4 posee dos átomos de hidrógeno, un átomo de azufre y cuatro átomos de oxígeno.
- 12. Introducción a los compuestos orgánicos Nomenclatura, propiedades físicas y representación de su estructura. • Si se va a hablar de los compuestos orgánicos es necesario saber cómo llamarlos. Primero, aprenderemos cómo se denominan los alcanos, porque sus nombres forman la base para los nombres de casi todos los compuestos orgánicos. Los alcanos se componen sólo de átomos de carbono y de hidrógeno y tienen únicamente enlaces sencillos.
- 14. Los HIDROCARBUROS son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno. La estructura molecular consiste en un armazón de átomos de carbono a los que se unen los átomos de hidrógeno.
- 15. • ALCANOS • Hidrocarburos saturados acíclicos. • Compuestos por enlaces sencillos C-C y C-H. • Carbono sp3 • Formula General: CnH2n+2 • Saturados completamente con H •ALCANOS LINEALES •Se nombran mediante un prefijo que indica el número de átomos de carbono de la cadena y el sufijo –ano. El más sencillo de los hidrocarburos, es el metano que está formado por un solo átomo de carbono unido a 4 átomos
- 16. Es necesario recordar los nombres de los primeros cuatro miembros, los nombres de los miembros restantes tienen prefijos griegos que indican el número de átomos de carbono en las moléculas.
- 17. • HIDROCARBUROS ALIFATICOS INSATURADOS ALQUENOS U OLEFINAS • Contienen un doble enlace (- C = C -) por molécula, los más sencillos. • Las raíces de los nombres derivan de los alcanos que tienen igual número de carbonos que la cadena más larga que contiene el doble enlace. • En la nomenclatura sistemática IUPAC se añade el sufijo –eno a la raíz característica. • El más simple es el eteno, formado por 2 átomos de carbono y cuatro de hidrógeno. • En cadenas de cuatro o más átomos de carbono, se debe buscar la cadena de carbono más larga que contenga al doble enlace. • Fórmulas generales de los alquenos C Fórmulas generales de los alquenos C
- 18. • ALQUINOS O HIDROCARBUROS ACETILENICOS • Contienen triples enlaces carbono-carbono (-C ≡ C -). • Se nombran siguiendo las mismas reglas que se usaron para los alquenos, añadiendo a la raíz característica de los alcanos correspondientes el sufijo – INO. • El triple enlace tiene preferente preferente posición posición con respecto respecto a los sustitutos sustitutos de la cadena de carbono, se le asigna el número más bajo posible al nombrarlo. • Fórmulas generales de los alquinos: C n H2n-2
- 20. OBSERVEN:
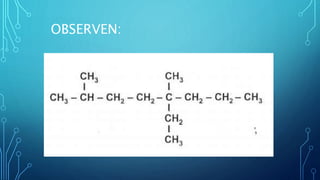
- 21. OBSERVEN: