Biochimie structurale Glucides-ESEF_UIK_Nihal.pptx
- 1. Université Ibn Tofail de Kenitra Ecole Supérieure de l’Education et de Formation (ESEF) Licence d’éducation : Spécialité Enseignement Secondaire- Sciences de la vie et de la terre واألرض الحياة علوم- الثانوي التعليم تخصص :التربية في اإلجازة Biochimie Structurale BIOCHIMIE STRUCTURALE
- 2. Biochimie Structurale Discipline (s) : BIOLOGIE, GEOLOGIE, SCIENCES DE L’EDUCATION, TIC Spécialité(s) du diplôme : Sciences de la Vie et de la Terre Mots clés : ENSEIGNEMENT, BIOLOGIE, GEOLOGIE, DIDACTIQUE, SCIENCES DE L’EDUCATION Licence d’éducation : Spécialité Enseignement Secondaire- Sciences de la vie et de la terre
- 3. Biochimie Structurale Semestre Numéro du module Intitule du module VH (Heures) Nature du module Langue d’enseignement S1 M01 Biologie cellulaire 50 Disciplinaire Français S2 M15 Biochimie structurale 50 Disciplinaire Français S2 M16 Génétique I 50 Disciplinaire Français Licence d’éducation : Spécialité Enseignement Secondaire- Sciences de la vie et de la terre
- 4. Biochimie Structurale Licence d’éducation : Spécialité Enseignement Secondaire- Sciences de la vie et de la terre 1. LES OBJECTIFS DE LA FORMATION • Approfondissement/Acquisition des savoirs et savoir-faire relatifs aux Sciences de la Vie et de la Terre ; • Acquisition des connaissances de base en éducation, en pédagogie et en didactique de la (les) disciplines ; • Usage des technologies éducatives ; • Acquisition des techniques d’animation et de communication ; • Acquisition des fondamentaux et de la déontologie du métier d’enseignement ; • Connaissance du milieu professionnel ; • Acquisition des capacités de l’auto-formation.
- 5. Biochimie Structurale Licence d’éducation : Spécialité Enseignement Secondaire- Sciences de la vie et de la terre 2. COMPETENCES AACQUERIR Le lauréat de la licence en éducation, option enseignement secondaire, sera en mesure de poursuivre une formation qualifiante dans l’enseignement public ou privé, ou bien poursuivre ses études supérieures, en mobilisant ses compétences disciplinaires, linguistiques, communicatives, pédagogiques, didactiques et technologiques acquises dans les différents modules. 3. DEBOUCHES DE LA FORMATION La licence d’éducation spécialité SVT permet aux étudiants : - De se présenter à un certain nombre de formations à caractère professionnel ou académique - D’être candidats au métier de l’enseignement des Sciences de la Vie et de la Terre; - De poursuivre les études de type Masters et Masters spécialisés en Enseignement des SVT, proposés par les Universités Marocaines et éventuellement continuer des études doctorales.
- 6. N° d’ordre du module M15 Intitulé du module BIOCHIMIE STRUCTURALE Nature du module Disciplinaire Langue Français Semestre d’appartenance du module S3 Biochimie Structurale BIOCHIMIE STRUCTURALE DESCRIPTIF DU MODULE
- 7. COMPÉTENCES VISÉES Au terme du module de Biochimie structurale, les étudiants s’approprient les savoirs et savoir-faire relatif aux constituants organiques et minéraux du vivant, et seront en mesure de les réinvestir pour résoudre des problèmes scientifiques liés à ce module et à des modules ultérieurs de Biologie. OBJECTIFS Au terme de ce module, l'étudiant sera en mesure de : Décrire les structures chimiques des différents composants organiques et inorganiques du vivant (eau et sels minéraux, glucides, lipides, acides aminés, protéines et acides nucléiques). S’approprier des manipulations de laboratoire qui permettent : - L’identification des glucides ; - L’extraction d’ADN d’un tissu végétal ; - La séparation des acides aminés d’un mélange par chromatographie. Biochimie Structurale BIOCHIMIE STRUCTURALE 1.1. COMPÉTENCES ET OBJECTIFS DU MODULE
- 8. Biochimie Structurale BIOCHIMIE STRUCTURALE M01 (Biologie cellulaire), M06 (Chimie 1),M13 (Chimie 2) 1.2. PRÉREQUIS PÉDAGOGIQUES 1.3. VOLUME HORAIRE (Les travaux dirigés et les travaux pratiques sont obligatoires dans les modules Disciplinaires et les modules Métiers, quand la nature disciplinaire de ces modules les exige. Les travaux pratiques, hors stage d’immersion, constituent 20% au minimum du volume horaire global du module nécessitant des travaux pratiques). Composante(s) du module Volume horaire (VH) Cours TD TP Activités Pratiques Travail personnel Evaluation (évaluation des connaissances et examen final) VH global 22h 8h 16h 4h 50 h VH global du module 22h 8h 16h 4h 50 h % VH 44% 16% 32% 8% 100%
- 9. Biochimie Structurale BIOCHIMIE STRUCTURALE 1.4. DESCRIPTION DU CONTENU DU MODULE (COURS) Partie 1 : Structure et propriétés de l’eau et des sels minéraux 1. Rôles biologiques de l’eau 2. Propriétés physicochimiques de l’eau Partie2 : Structure et propriétés des glucides 3. Les oses : Plan de base des oses, appellation des oses, diversité, filiation, conformation spatiale, propriétés physico- chimique, intérêt biologique. 4. Les oligosides : Liaison 0-glycosidique, diversité d’enchainement, convention d’écriture, analyse structurale des oligosaccharides 5. Les polysaccharides : perméthylation des homopolysaccharides et hétéropolysaccharides, détermination de leur structure 6. Les hétérosides Partie 3: Structure et propriétés des lipides 7. Les acides gras : structure chimique, nomenclature, nombre d’atome de C, nombre de doubles liaisons, numéros d’atomes de C qui portent les doubles liaisons, propriétés physico-chimiques, configuration des doubles liaisons, acides gras saturés, acides gras non saturés 8. Les acylglycérols : formules développées et nomenclature, propriétés, hydrolyse 9. Principaux constituants des membranes biologiques : phosphoglycérides, sphingolipides, stérols, stéroïdes et dérivés de Terpènes
- 10. Biochimie Structurale BIOCHIMIE STRUCTURALE Partie 4: Structure et propriétés des amino-acides et des protéines 1. Les acides aminés : structure, nomenclature, propriétés physico-chimique, méthode de détection, dosage 2. Les Peptides : liaison peptidique, méthode d’analyse de la séquence peptidique, étude de quelques peptides importants 3. Les protéines : propriétés physico-chimiques, structure tridimensionnelles, conformationnelle et ordonnée, fractionnement (purification et extraction). Partie 5: Structure et propriétés des acides nucléiques 1. Constituants des acides nucléiques : ADN, ARN, Bases azotées et leurs propriétés, les nucléosides, les nucléotides 2. Structure des acides nucléiques : structure primaire et polymérisation, structure secondaire de l’ADN et ARN, structure tertiaire de l’ADN 3. Caractéristiques physico-chimiques et fonctionnelles de l’ADN : propriétés physico-chimiques, méthodes d’étude, conservation de l’information génétique 4. Types et caractéristiques des ARN : différents types d'ARN, fonction et rôle, transcription et traduction, notion de code génétique Travaux dirigés - Structure et propriétés des oses et de leurs dérivés - Structure et propriétés des lipides - Acides aminés et protéines : structures, conformations & propriétés - Acides nucléiques : structures et propriétés Travaux pratiques – Identification des sucres – Séparation des acides aminés d’un mélange par chromatographie et détermination du pHi – détermination de l’indice de saponification d’un lipide (Huile de ricin par exemple) – Extraction de l’ADN d’oignon – Propriétés physique des acides nucléiques : spectre d’absorption
- 11. Biochimie Structurale BIOCHIMIE STRUCTURALE 1.5. Objectifs du module Connaitre les notions chimiques fondamentales et les structures biochimiques. Comprendre l’intérêt des structures moléculaires et des réactions chimiques telles qu’elles se déroulent in vitro. Mettre en relation les structures avec les réactions biochimiques in vivo. 1. 6. Objectifs du cours Restituer la structure des principaux glucides et dérivés. Distinguer les principales propriétés chimiques et physiques des glucides. Connaitre l'importance biologique des glucides.
- 12. Biochimie Structurale BIOCHIMIE STRUCTURALE Examen de fin de semestre : épreuve écrite ; Contrôles continus : tests, épreuves orales, devoirs, exposés ou autre moyen de contrôle ; Travaux pratiques : rapports de TP. - Contrôles continus : 20% - Examens des travaux pratiques : 20% - Examen final : 60% 2. PROCEDURES D’EVALUATION 2.1. Modes d’évaluation 2.2. Note du module (Préciser le pourcentage des différentes évaluations de module pour obtenir la note du module.) Évaluation connaissances en Biochimie: QCM (20 questions) et deux questions de développement
- 13. Biochimie Structurale BIOCHIMIE STRUCTURALE I. Biochimie: historique et définitions •Historique: – Chimie biologique ou chimie des êtres vivants – Origines « chimiques » au XVIIIesiècle: Lavoisier – Origines « biologiques » au XIXe: Lamarck •Langage commun de toutes les sciences biologiques: –Biologie cellulaire –Physiologie –Génétique, pharmacologie, microbiologie,…
- 14. la biochimie étudie: Étude de la matière vivante Étude des réactions chimiques des cellules Étude des substances organiques et des réactions chimiques sous-tendant le processus de la vie Étude de la structure et la conformation des molécules organiques et de leurs réactions chimiques : dégradation et biosynthèse. Intégrer les données obtenues à l'échelle moléculaire afin de les intégrer dans des niveaux d'organisation supérieur (cellule → tissu → organe → organisme) Les molécules présentes dans les cellules et les organismes vivants Les réactions et transformations subites par ces molécules Les biochimistes font appel à d'autres connaissances issues d'autres disciplines o Nomenclature de la chimie organique o Cinétique chimique o Thermodynamique o Physique o Informatique Biochimie Structurale BIOCHIMIE STRUCTURALE
- 15. Biochimie Structurale BIOCHIMIE STRUCTURALE (Entre parenthèse) Santé : équilibre harmonieux des réactions biochimiques de l’organisme; Maladie: reflet des anomalies des molécules biologiques, de réactions biochimiques ou de processus biochimiques Examens biochimiques: partie intégrante du diagnostic et du suivi de traitement de nombreuses pathologies –Diabète –Hyperlipidémies –Maladie rénale…. Connaissances en biochimie: indispensables pour une pratique des sciences biomédicales
- 16. Biochimie structurale (En résume) • Étude de la structure d’une molécule Décrire organisation des atomes en groupe fonctionnel, les liaisons chimiques , l’isomérie moléculaire … Expliquer ses interactions avec le milieu intérieur et avec les autres molécules • Etude des propriétés physicochimiques Utilisées dans les techniques mises au point pour étude des molécules : extraction, purification, caractérisation, reconstitution et dosage BIOCHIMIE STRUCTURALE Biochimie Structurale
- 17. De formule chimique H2O, l’eau est le constituant majeur de la cellule et donc de la matière vivante (60-95% en fonction des êtres vivants). Il s’agit d’une molécule polaire constituant un dipôle, l’oxygène étant très électronégatif et l’hydrogène électropositif. Ainsi, les molécules d’eau auront tendance à établir entre elles des liaisons hydrogène transitoires conférant à l’eau liquide une structure réticulaire fluide. Grâce à ses propriétés physico-chimiques, l’eau est capable de solubiliser les molécules polaires et les ions ce qui en fait le principal solvant des liquides biologiques (cytosol, plasma sanguin etc.). Fondamentale dans les processus biochimiques de la cellule, l’eau joue aussi un rôle de régulateur thermique. BIOCHIMIE STRUCTURALE L’eau Partie 1 : Structure et propriétés de l’eau et des sels minéraux 1. Rôles biologiques de l’eau
- 18. BIOCHIMIE STRUCTURALE L’eau Partie 1 : Structure et propriétés de l’eau et des sels minéraux 1. Rôles biologiques de l’eau L’eau est la source de la vie. Calculons cette éléctronégativité pour l’eau : EN = 1,4. L’eau possède donc 2 liaisons covalentes et c’est ce type de liaison qui va expliquer pas mal ses propriétés. Par exemple, la température d’ébulliton est très élevée pour les atomes de la 1ère ligne car ils possèdent des liaisons covalentes. Lorsque des molécules possèdent des liaisons covalentes, des ponts hydrogènes apparaissent entre les différentes molécules : ces ponts H sont toujours en mouvement, leur durée de vie est en moyenne de 10−12s. Cette liaison électrostatique se fait entre un noyau d’hydrogène chargé positivement et le nuage éléctronique entourant le noyau d’oxygène. Lorsque nous chauffons ce type de molécules, il faut d’abord rompre les ponts H et donc apporter plus d’énergie pour faire bouillir ces molécules ce qui explique la température d’ébullition élevée.
- 19. Partie 1 : Structure et propriétés de l’eau et des sels minéraux 2. Propriétés physicochimiques de l’eau 2. 1. Solvant universel L’eau est le solvant universel, c’est cette propriété qui a permis le vie. L’eau n’est pas un solvant pour tout et heureusement. En effet, il est impossible de dissolver une molécule polaire dans une apolaire donc seules les molécules polaires sont solubles dans l’eau. Cette propriété est aussi très intéressante en biologie. BIOCHIMIE STRUCTURALE L’eau 2. 2. Tension de surface La tension de surface, force existante au niveau de toute interface entre 2 surfaces différentes, de l’eau est très élevée due à ses liaisons polaires. Cela a comme conséquence que les membranes élastiques ne se rompent pas mais cela explique aussi pourquoi l’eau se met sous forme de sphère (tendance à prendre le moins de place possible). En sortant du ventre de notre maman, grâce à une molécule, appelée le surfactant, diminuant la tension superficielle, nos alvéoles peuvent s’ouvrir et nous pouvons donc respirer.
- 20. L’eau BIOCHIMIE STRUCTURALE 2. 3. Adhérence et cohésion Adhérence : s’accrocher à quelque chose de proche, cela est possible entre molécules possédant des liaisons polaires car des ponts H se forment. Cette adhérence dépend de la tension de surface ; ainsi plus la tension de surface sera grande plus l’adhérence le sera aussi. Cohésion : gouttes d’eau attachées les unes aux autres. Une des conséquences majeures de ces propriétés est la montée de la sève dans les arbres. Pour que l’eau monte, elle s’accroche aux parois (adhésion) et grâce à la cohésion entre ses molécules, elle peut monter dans le tronc. 2. 4. Chaleur spécifique Température = mesure de l’agitation des molécules. Comme l’eau est une molécule polaire, il faut d’abord casser les liaisons hydrogènes pour augmenter la température, pour permettre aux molécules de bouger les unes par rapport aux autres. Cette propriété permet à la Terre de garder une température constante (petite variation seulement) car la Terre est recouverte majoritairement d’eau.
- 21. 2. 5. Chaleur de vaporisation La chaleur de vaporisation est déterminée par la quantité d’énergie à apporter pour transformer 1kg d’une substance de l’état liquide à celui gazeux. Comme l’agitation moléculaire des gaz est importante, il faut casser les ponts H ce qui demande un gros apport d’énergie. La transpiration nous permettant de garder notre température constant (homéostasie) est une illustration de cette propriété. 2. 6. Température de fusion Le point de congélation est élevé car l’eau est polaire. Vu que les ponts H se solidifient, l’eau prend plus de place à l’état solide qu’à l’état liquide mais la masse volumique de la glace est plus faible que celle de l’eau et c’est pour ca qu’elle flotte sur l’eau. L’eau BIOCHIMIE STRUCTURALE
- 22. Les Sels Minéraux Les sels minéraux sont des substances retrouvées soit sous forme mobilisée (cas des os) soit sous forme dissociée en ions (atome ou groupe d’atomes ayant perdu sa neutralité électrique : Na+, Ca2+, H+, Cl- etc.) lorsqu’ils sont en solution. Les ions chargés positivement sont nommés cations et ceux chargés négativement anions. Entre eux, ou avec les molécules d’eau, les ions établissent des liaisons ioniques (liaisons faibles de type électrostatique). Leurs concentrations sont étroitement régulées pour assurer le maintien de l’homéostasie (équilibre de fonctionnement) cellulaire. BIOCHIMIE STRUCTURALE L’eau
- 23. Glucides BIOCHIMIE STRUCTURALE 1. Introduction 2. Caractères généraux des glucides 2.1. Définition 2.2. Classification des glucides 3. Les monosaccharide 3.1. Définition 3.2. Classification des oses 3.3. Structure linéaire des oses 3.4. Structure cyclique des oses
- 24. Glucides BIOCHIMIE STRUCTURALE 1. Introduction • Glucose: terme né en 1838 du grec glukus« doux » • Glucides : biomolécules naturelles les plus abondantes sur la planète Autre dénomination: sucres, saccharides, hydrates de carbones (abandonné) • Multiples rôles des glucides: - Énergétique, Structural, Métabolique, Fonctionnel
- 25. BIOCHIMIE STRUCTURALE 2. Caractères généraux des glucides Sont les biomolécules les plus abondantes dans la matière vivante. Ils représentent : Environ 70 % du poids sec des végétaux Environ 5 % du poids sec des animaux. Leur formule brute générale : (CH2O)n/CnH2nOn Partie importante de notre alimentation riz, pain, pomme de terre, lait… Glucides
- 26. BIOCHIMIE STRUCTURALE 2.1. Définitions et rôles des glucides Ce sont des polyalcools qui comportent une fonction aldéhyde ou cétone. La plupart des glucides sont des composés ternaires (contiennent C, H et O), Mais certains peuvent contenir de l’azote, du phosphore ou du soufre. Le représentant majeur des glucides est le glucose : • Principal carburant des tissus • Rôle fondamental car tous glucides alimentaires sont absorbés sous forme de glucose ou convertis en glucose dans le foie. •Tous les glucides sont synthétisés à partir du glucose. Glucides
- 27. BIOCHIMIE STRUCTURALE a. Rôle énergétique 50 % de calories apportées par l’alimentation sont des glucides. Réserve énergétique sous forme polymérisée : glycogène et amidon chez les animaux et les végétaux. b. Rôle structural Eléments de structure des cellules : cellulose chez les végétaux, mucopolysaccharides chez les animaux. Eléments de reconnaissance et de communication entre cellules (polyosides des groupes sanguins….). Constituants de la structure de nombreuses macromolécules biologiques fondamentales : glycoprotéines, acides nucléiques (ribose et désoxyribose), coenzymes et antibiotiques. c. Métabolique La glycolyse d. Fonctionnel Hormones Glucides
- 28. BIOCHIMIE STRUCTURALE 2.2. Classification des glucides Se répartissent en 2 groupes Sucres simples : OSES = monosaccharides (non hydrolysables) --ALDOSES (C1) --CETOSE (C2) Glucides complexes : OSIDES (hydrolysables) Selon le degré de polymerisation, on distingue: --HOLOSIDES : Oligosides = Oligosaccharides : 2 à 10 unités Polyosides = Polysaccharides : chaînes à plus de 10 unités. --HÉTÉROSIDES : Association de plusieurs molécules d’oses avec une fraction non glucidique appelée aglycone. types de molécules ( lipides, protéines…) -- DÉRIVÉS D'OSES: molécules d'oses ayant subi des réactions chimiques ( oxydations, réductions ) sur une de leur fonction Glucides
- 29. BIOCHIMIE STRUCTURALE 2.2. Classification des glucides Les Oses ■ Oses: Aldéhydes ou Cétones polyhydroxylées la nature de la fonction carbonyle réductrice (aldéhyde ou cétone) le nombre d’atomes de carbones de la chaîne (3 à 8 C). (n-1) fonction alcool (primaire, secondaire) Aldéhyde Aldose Cétone Cétose 3C = Triose Aldotriose Cétotriose 4C = Tétrose Aldotétrose Cétotétrose 5C = Pentose Aldopentose Cétopentose 6C = Hexose Aldohexose Cétohexose Glucides
- 31. BIOCHIMIE STRUCTURALE Glucides 2.2. Classification des glucides Structure des Oses CH2 OH CHOH CHOH CHOH C O H CH2 OH C=O CHOH CHOH CH2 OH 1 2 3 4 5 1 2 3 4 5 Aldopentose Cetopentose
- 32. BIOCHIMIE STRUCTURALE 3. Structure linéaire des oses 3.1 chiralité et isomerie a-Isomérie plane Isomères de constitution même formule brute mais propriétés physico-chimiques différentes. Ex : D-Glucose et D-fructose Isomères de position même formule brute mais groupe fonctionnel occupe une position différente sur le même squelette carboné. Ex: D-Glucose et D-Galactose (position différente de OH en C4. On appelle épimère deux oses qui ne diffèrent l’un de l’autre que par la configuration d’un seul et même carbone. Ex : D-glucose et D-mannose sont épimères en C2. Ex : D-glucose et D-galactose sont épimères en C4. Glucides
- 33. BIOCHIMIE STRUCTURALE b-Isomérie optique Les molécules comportant des C asymétriques ont une activité optique : elles ont un pouvoir rotatoire, donc capables de dévier le plan de la lumière polarisée. Ces isomères optiques ont les mêmes propriétés chimiques et physiques sauf leur pouvoir rotatoire spécifiques qui sont égaux en valeur absolue mais de signes contraires. Si la lumière polarisée est dérivée vers la droite : la substance est dite dextrogyre et notée (+), vers la gauche: la substance est dite lévogyre et notée (-) Glucides
- 34. BIOCHIMIE STRUCTURALE La notion de pouvoir rotatoire est liée à l’existence dans la molécule d’un ou plusieurs carbones asymétriques * * Exemple : le glyceraldéhyde CH2 OH CHO *CHOH Glyceraldéhyde CH2 OH CHO C HO H D-Glyceraldéhyde CH2 OH CHO C HO H L-Glyceraldéhyde Glucides
- 35. BIOCHIMIE STRUCTURALE Remarques Si un ose possède (n) carbones asymétriques, il aura 2n stéréoisomères possibles Ex : aldohexose à 4 carbones asymétriques aura 24 soit 16 stéréoisomères Un ose de la série D peut être dextrogyre ou lévogyre ; il en est de même des oses de la série L. En général les oses naturels sont de la série D. Les oses ayant un plan de symétrie ne dévient pas la lumière polarisée, même s’ils ont un ou plusieurs carbones asymétriques. Glucides
- 36. C C C C C O H O C H H HO HO HO HO H H H Ex : Acide mucique (dérivé du galactose) Plan de symétrie Glucides BIOCHIMIE STRUCTURALE
- 37. Les oses de la série D et de la série L sont images les uns des autres dans un miroir. D-Glucose CH2 OH C OH C OH H CHO H H C OH HO C H MIROIR CH2 OH HO C C OH H CHO H H C OH HO C H L-Glucose BIOCHIMIE STRUCTURALE Glucides
- 38. 3.2. Filiation des aldoses Selon Kiliani et Fisher, les additions de carbones se font au dessus du carbone n°1 ; Cela aboutit à un couple d’épimères. D-Glycer aldéhyde CH2 OH CHO C OH H CH2 OH CHOH C OH H CΞN CH2 OH CHOH C OH H COOH CH2 OH CHOH C OH H CHO + HCN + 2H2O NH3 + 2H H2O CH2 OH C OH C OH H CHO H D-Erythrose CH2 OH C H C OH H CHO HO D-Thréose Glucides BIOCHIMIE STRUCTURALE
- 39. Erythrose et thréose sont épimères en C2 Glucose et mannose épimères en C2 Glucose et galactose épimères en C4 L’absence d’épimérase empêche la transformation du Galactose en Glucose et entraîne une des formes de la galactosémie congénitale du nouveau-né. Glucides BIOCHIMIE STRUCTURALE
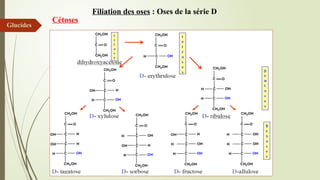
- 40. Filiation des oses : Oses de la série D Aldoses
- 41. 3.3. Filiation des cétoses Les cétoses sont nommés en ajoutant la désinence « UL » au nom de l’aldose correspondant Exemple : Ribose => Ribulose Le passage des aldoses aux cétoses se fait grâce à des isomérases. Glucides BIOCHIMIE STRUCTURALE
- 42. Filiation des oses : Oses de la série D Cétoses Glucides
- 43. 4. Représentations cycliques 4.1.Hémiacétal et mutarotation Mise en évidence de l’existence de la structure cyclisée du glucose Réaction au réactif de Schiff Le glucose possède une fonction aldéhydique. En présence du réactif de Schiff, on devrait obtenir une coloration rouge que on n’obtient pas. Réaction d’hémiacétalisation en présence d’un alcool Une molécule d’aldéhyde comme une cétone est capable de réagir successivement avec deux molécules d’alcool. Aldéhyde + méthanol →hémiacétal Hémiacétal + méthanol →acétal + eau Dans les mêmes conditions, le glucose ne réagit qu’avec une seule molécule de méthanol BIOCHIMIE STRUCTURALE Glucides
- 44. Explication : Dans le glucose, il s’est produit une réaction entre la fonction aldéhydique et un des groupements OH (= réaction d’hémiacétalisation intramoléculaire). Ceci expliquerait pourquoi le glucose n’est pas capable de colorer le réactif de Schiff et pourquoi il ne peut réagir qu’avec une seule molécule de méthanol (puisqu’il aurait déjà réagi avec une fonction alcool pour se retrouver sous la forme d’un hémiacétal). Glucides BIOCHIMIE STRUCTURALE
- 45. Phénomène de mutarotation La cristallisation du D-glucose dans des solvants conduit non pas à un seul produit mais à 2 produits dont les pouvoirs rotatoires sont différents. Ces 2 formes ont été qualifiées de forme α (+ 112), et de forme β (+19°). Ces deux formes sont dites anomères. il se produit un changement de conformation entre les deux formes en solution. En fait, la mutarotation correspond au passage d’une forme anomérique à une autre par ouverture du glucose sous forme hémiacétalique et recyclisation. (β-D-glucose glucose linéaire α-D-glucose). ⇔ ⇔ Glucides BIOCHIMIE STRUCTURALE
- 46. 4.2. Pont oxydique et formule de TOLLENS Forme cyclique Tollens : hydratation de l’ose puis déshydratation) Ex : glucose D-Glucose CH2 OH C OH C OH H CHO H H C OH HO C H HO C H CH2 OH C OH C OH H C OH H H C OH OH H HO C H CH2 OH C OH C H C H H C OH OH H O Pont oxydique C1- C5 D-Glucopyranose +H2O H2O Glucides BIOCHIMIE STRUCTURALE
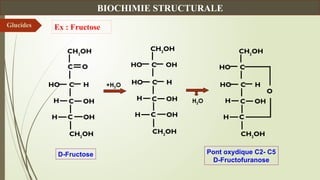
- 47. CH2 OH C OH C OH H CH2 OH H C O HO C H CH2 OH C OH C OH H CH2 OH H HO C OH HO C H CH2 OH C OH C H CH2 OH H HO C HO C H O D-Fructose Pont oxydique C2- C5 D-Fructofuranose Ex : Fructose +H2O H2O Glucides BIOCHIMIE STRUCTURALE
- 48. Remarques Pour les alohexoses, la forme pyranique est la plus stable. Pour les cétohexoses et les pentoses, c’est la forme furanique qui est la plus stable. Apparition donc d’un nouveau carbone asymétrique C1 (aldoses) et C2 (cétoses) : Carbones anomériques Le phénomène de mutarotation implique l'existence d'un carbone asymétrique supplémentaire. La formation d'hémiacétal implique que la fonction réductrice a déjà établit une liaison avec un alcool. Glucides BIOCHIMIE STRUCTURALE
- 49. Structures de Haworth Cyclisation entre C1 et C5 ou entre C1 et C4 pour les aldoses Cyclisation entre C2 et C6 ou entre C2 et C5 pour les cétoses Deux possibilités de cyclisation: Glucides BIOCHIMIE STRUCTURALE
- 50. Remarques Dans la série D, si le carbone terminal est extérieur au cycle, il est orienté vers le haut. C’est l’inverse dans la série L. Dans la forme α, l’hydroxyle anomérique est toujours en position trans par rapport au dernier carbone extérieur au cycle. Cette position est cis dans la forme β. -D-Glucopyranos α e -D-Fructofuranos β e Glucides BIOCHIMIE STRUCTURALE
- 51. II.4.4. Formule de REEVES La forme chaise : Plan équatorial contenant les carbones 2, 3, 5 et l’atome d’oxygène. C4 est au dessus du plan et C1 en dessous. C’est la forme stable des oses naturels. La forme bateau : Ce sont les mêmes plans mais C1 et C4 sont au dessus Glucides BIOCHIMIE STRUCTURALE
- 52. II.5. Propriétés des oses II.5.1. Propriétés physiques Solides blancs, cristallisés, sucrés Très solubles dans l’eau Insolubles dans les solvants apôlaires Doués d’activité optique en solution Leur structure est thermo dégradable (caramélisation) Glucides BIOCHIMIE STRUCTURALE
- 53. II.5.2. Propriétés chimiques des oses Propriétés de la fonction carbonylée En milieu alcalin et à froid, les oses subissent une interconversion et une épimérisation. Glucides BIOCHIMIE STRUCTURALE
- 54. CH2 OH C C CHO C C CH2 OH C C COOH C C D-Glucose Acide gluconique + H2 O + I2 + 2 H I Réactions d’oxydation Oxydation douce par l’iode Aldoses acides aldoniques les cétoses ne sont pas oxydés dans ces conditions mannose acide mannonique galactose acide galactonique BIOCHIMIE STRUCTURALE Glucides
- 55. Oxydation énergique Avec l’acide nitrique Donne un diacide appelé acide aldarique ou saccharique possédant une fonction carboxyliques sur le C1 et le C6 CH2 OH C C CHO C C COOH C C COOH C C Acide nitrique D-Glucose Acide glucarique le galactose donne l'acide galactarique Glucides BIOCHIMIE STRUCTURALE
- 56. Si la fonction aldéhyde est protégée pendant l'oxydation, on obtient les acides uroniques oxydés uniquement sur la fonction alcool primaire : Formation d’acides uroniques (Acide glucuronique), précurseur de la voie de synthèse de la vitamine C. CH2 OH C C CHO C C COOH C C CHO C C Acide nitrique D-Glucose Acide glucuronique - Le glucose donne Ac. Glucoronique - le galactose donne l'acide galacturonique Glucides BIOCHIMIE STRUCTURALE
- 57. Oxydation par l’acide périodique Clivage oxydatif du cycle Coupures entre carbones portant OH libres Permet la détermination de la nature du cycle Furanose → simple dialdéhyde Pyranose → dialdéhyde + acide formique (HCOOH) Glucides BIOCHIMIE STRUCTURALE
- 58. Réactions de réduction Par action d’un borohydrure alcalin (LiBH4 ou NaBH4) Transformation aldéhydes et cétones en polyalcools ou itols A partir d’un aldose → un type de polyol A partir d’un cétose → 2 polyols épimères en C2 La fonction aldéhydique ou cétonique est réduite en alcool Glucose Glucitol (ou Sorbitol) Galactose Galactitol (ou Dulcitol) Mannose Mannitol Ribose Ribitol Le Fructose donne 2 polyols car la réduction du C= O entraîne la formation d’un *C asymétrique Glucides BIOCHIMIE STRUCTURALE
- 59. Ex : D-Mannose (aldose) CH2 OH C C C C C H O CH2 OH C C CH2OH C C D-Mannose D-Mannitol + NaBH4 Glucides BIOCHIMIE STRUCTURALE
- 60. Ex : fructose (cétose) CH2 OH C C CH2OH C C O CH2 OH C C CH2OH C C OH H CH2 OH C C CH2OH C C HO H + NaBH4 D-Sorbitol D-Mannitol Glucides BIOCHIMIE STRUCTURALE
- 61. • Réaction à la liqueur de fehling Mettre en évidence le pouvoir réducteur des oses L’ion cuivrique Cu2+, de couleur bleue, est réduit en ion cuivreux Cu+ par le groupement carbonyle des oses pour donner de l’oxyde cuivreux Cu2O de couleur rouge qui précipite. Glucides BIOCHIMIE STRUCTURALE
- 62. Réactions d’addition et de substitution L’action des alcools sur les oses donnent des composés méthylés (ex : D méthyl glucoside). Formation d’osides par liaison osidique ou glycosidique O HOH2C CH2OH OH O HOH2C CH2OH O-CH3 + CH3OH α-D-Fructofuranose Méthyl-α-D-Fructofuranoside Glucides BIOCHIMIE STRUCTURALE
- 63. Perméthylation : Le sulfate de méthyle agit en substituant tous les hydrogènes des OH par un -CH3 formant ainsi un éther.. O HOH2C CH2OH OH O H3C-OH2C CH2O-CH3 O-CH3 O-CH3 H3C-O + (CH3)2SO4 -D-Fructofuranose Pentaméthyl-1,2,3,4,6 O-méthyl a-D-Fructofuranoside Cette réaction permet de mettre en évidence les fonctions alcools libres. Propriétés de la fonction alcool Glucides BIOCHIMIE STRUCTURALE
- 64. • Formation d’esters Par condensation avec des acides. Phosphoriques, on obtient des esters phosphoriques O HOH2C CH2OH OH Fructose O P-OH2C CH2O-P OH P = - H2PO3 Fructose 1- 6 bisphosphate + 2 H3PO4 BIOCHIMIE STRUCTURALE Glucides
- 65. Formation de sucres désoxy Sucres obtenus par réduction d’un ou de plusieurs hydroxyles O HOH2C OH OH OH 1 2 O HOH2C OH OH H 1 2 a-2-désoxy- D-ribose a-D-ribose Réduction de OH de C2 Glucides BIOCHIMIE STRUCTURALE
- 66. Contiguité de fonction alcool et carbonyle Formation osazones Action phénylhydrazine D-Glucose CH2 OH C OH C OH H CHO H H C OH HO C H D-Glucose phénylhydrazone CH2 OH C OH C OH H HC= H H C OH HO C H N-NH-H5C6 + H2O A froid + H2N-NH-H5C6 Milieu acétique Glucides BIOCHIMIE STRUCTURALE
- 67. Formation osazones par fixation de 2 molécules de phénylhydrazine A chaud D-Glucose CH2 OH C OH C OH H CHO H H C OH HO C H D-Glucosazone CH2 OH C OH C OH H HC= H C HO C H N-NH-H5C6 =N-NH-H5C6 + Acide phénylacétique + 3 x H2N-NH-H5C6 Milieu acétique glucose, mannose et fructose donnent le glucosazone. Application : Identification oses dans liquides biologiques. Glucides BIOCHIMIE STRUCTURALE
- 68. Oses d’importance biologique Les pentoses Le xylose : abondant dans les produits d’hydrolyse du bois, non métabolisé dans l’organisme humain. L’arabinose : sucre essentiellement végétal (gommes, fruits), peu métabolisé par humain mais excrété dans l’urine. Le D-Ribose : Rare à l’état libre ou en association avec d’autres oses. Présent dans toutes les cellules à l’état combiné avec l’acide phosphorique et des bases azotées pour former les nucléotides. Glucides BIOCHIMIE STRUCTURALE
- 69. Les hexoses Les plus importants, métabolisés par l’organisme humain : D-Glucose : présent dans toutes les cellules, à l’état libre et condensé et dans de nombreux liquides de l’organisme. D-Mannose : fréquent dans les osides végétaux et les lipides complexes. D- et L-Galactose : le plus abondant après le glucose dans les combinaisons glucidiques et lipidiques. D-Fructose : abondant à l’état libre dans les fruits et le miel, très répandu dans l’ensemble des végétaux à l’état combiné. Glucides BIOCHIMIE STRUCTURALE
- 70. Les dérivés d’oses Les osamines Oses dont la fonction alcool en C2 est substituée par NH2ou N- acéthyl amine (NH-CO-CH2). Les plus importantes sont les galacto et glucosamine, ou N acétyl- glucosamine. Trouvés essentiellement dans : -sous forme polymérisée dans la chitine (squelette arthropodes) - la muréine (paroi des bactéries) -les glycoprotéines. NH2 NH-CO-CH3 -D-glucosamine α N-acétyl-α-D-glucosamine Glucides BIOCHIMIE STRUCTURALE
- 71. Acides uroniques Oxydation de la fonction alcool primaire(CH2OH) en fonction carboxylique(COOH): acide glucuronique ou glycuronate (forme de détoxication), acide galacturonique (pectines) Désoxyribose Qui dérive du ribose (la fonction alcool portée par le carbone 2 est absente) Glucides BIOCHIMIE STRUCTURALE
- 72. III. Les osides Polymères d'oses parmi lesquels on distingue : les hétérosides dont l'hydrolyse libère des oses et des composés non glucidiques(aglycone), Les holosides dont l'hydrolyse ne libère que des oses et parmi ceux-ci les oligosides et les polyosides dont la différence se situe au niveau du nombre de monomères formant le polymère. Les oligosides résultent de la condensation d'oses par formation entre chacun d'eux d'une liaison ester de type osidique ou glycosidique. Cette dernière se fait entre l'hydroxyle réducteur d'un ose porté par le carbone anomérique (C1pour aldoses et C2 pour cétoses); OH en position α ou ß, avec un hydroxyle d'un autre ose. Glucides BIOCHIMIE STRUCTURALE
- 73. III.1. Les oligosides Etude descriptive de quelques diholosides importants --- Le maltose Diholoside: produit de dégradation de l'amidon et du glycogène par les amylases. Par hydrolyse acide ou enzymatique par une maltase, il donne 2molécules de glucose. Les résidus de glucose sont libérés par hydrolyse chimique ou par l'α-D-glucosidase. C'est un sucre réducteur puisque l'hydroxyle du carbone anomère du second glucose est libre. α-D-glucopyranosyl (1-4) α-D-glucopyranose Glucides BIOCHIMIE STRUCTURALE
- 74. --- Le lactose Sucre du lait, propre au règne animal, synthétisé dans les glandes mammaires, résulte de la condensation entre un galactose et un glucose. L’hydrolyse enzymatique assurée par la lactase. diholoside reducteur. β-D-galactopyranosyl (1-4) α-D-glucopyranose ---Cellobiose Produit de dégradation de la cellulose, par hydrolyse, il donne 2 molécules de glucose. Il s’agit d’un diholoside reducteur: ß D-glucopyranosido (1-4) D-glucopyranose Glucides BIOCHIMIE STRUCTURALE
- 75. ---Le saccharose C’est un osido-oside que l’on trouve dans les végétaux. Produit intermédiaire de la photosynthèse. Il est mis en réserve dans les tiges de la canne à sucre et dans les racines des betteraves. Résulte de l’association d’un glucose et d’un fructose unis par leur groupement réducteur. diholoside non réducteur. α-D-glucopyranosyl (1-2) -D-fructofuranoside β Glucides BIOCHIMIE STRUCTURALE
- 76. DETERMINATION DE LA NATURE DES OLIGOSIDES --Nature oses constitutifs : hydrolyse acide et chromatographie --Mode de liaison des oses : Recherche du pouvoir réducteur. Si disaccharide réducteur => Liaison oside-ose Si non réducteur => liaison oside-oside --Position des hydroxyles impliqués : Perméthylation et d’hydrolyse, obtention d’oses méthylés identifiables par chromatographie. --Conformation de l’OH anomérique impliqué : Par hydrolyse enzymatique spécifique Si α-glycosidase => conformation α Si β-glycosidase => conformation β Glucides BIOCHIMIE STRUCTURALE
- 77. III.2. Les polyosides, Polysaccharides, glycanes L’amidon Polyoside de réserve glucidique végétal Alimentation (céréales, tubercules…) Haut polymère d’α-D-glucoses Amidon linéaire ou amylose : Liaisons en α (1→4) Conformation spatiale spiralée Amylopectine Ramifications α (1→6) Ramification tous les 10 à 12 résidus Glucides BIOCHIMIE STRUCTURALE
- 78. Le glycogène Polyoside de réserve du monde animal. Stocké au niveau du foie et du muscle Structure identique à celle de l’amidon, mais ramifications tous les 8 à 10 résidus Dégradation grâce aux phosphorylases et aux enzymes débranchantes. Glucides BIOCHIMIE STRUCTURALE
- 79. La cellulose Polyoside de structure du monde végétal Enchaînement de D-glucoses en β (1→4) L’organisme humain ne peut les dégrader Liaisons coupées par les cellulases de certaines bactéries de l’appareil digestif des ruminants avec libération de β-D-glucose Confère aux parois des cellules végétales leur rigidité. 50 % du bois 100 % du coton Glucides BIOCHIMIE STRUCTURALE
- 80. III.3. Les hétérosides Résultant de l’association du carbonyle d’un ose avec une fraction non glucidique Leur classification se fait selon la nature du groupement fonctionnel de l’aglycone impliqué dans la liaison osidique O-hétéroside : ose + hydroxyle (OH) alcoolique ou phénolique S-hétéroside : ose + groupement thiol (SH) N-hétéroside : ose + groupement NH2 Glucides BIOCHIMIE STRUCTURALE
- 81. III.4. Les Mucopolysaccharides (MPS) Polyosides hétérogènes, polymérisation de sous-unités disaccharidiques élémentaires Une molécule d’acide hexuronique Une molécule d’hexosamine porteuse ou non de plusieurs groupements sulfatés Ils ont un caractère acide très marqué Ils sont toujours unis à des protéines Glucides BIOCHIMIE STRUCTURALE
- 82. MPS de structure : Présents dans les tissus conjonctifs Acide hyaluronique Médecine physique : Restauration viscosité liquide synovial Médecine esthétique : Comblement des rides. La chondroïtine : Structure et propriétés voisines de celles de l’acide hyaluronique. Glucides BIOCHIMIE STRUCTURALE
- 83. III.5. Les Glycoprotéines (GCP) Union covalente d’une fraction glucidique (glycane) avec une fraction protéique Importance biologique Constituants des membranes plasmiques Constituants monosaccharidiques Oses neutres (D-galactose, D-xylose…) Osamines (D-glucosamine, D-galactosamine…) Acides uroniques (acide D-glucuronique) Acides sialiques (acide N-acétylneuraminique) Glucides BIOCHIMIE STRUCTURALE
- 84. Exemples de GCP GCP sériques Prothrombine : Rôle dans coagulation Transferrine : Transport du fer GCP des groupes sanguins GCP diverses : hormone lutéinisante (LH), hormone chorionique gonadotrope (HCG)… Glucides BIOCHIMIE STRUCTURALE
- 85. III.6. Les Glycolipides (GCL) Union covalente d’une fraction glucidique avec une fraction lipidique Existence de deux pôles Un pôle hydrophile : plus il est important, plus le glycolipide est soluble Un pôle hydophobe dû à la partie lipidique Glucides BIOCHIMIE STRUCTURALE
- 86. Exemples de GCL Les cérébrogalactosides : Liaison d’un alcool à longue chaîne (sphingosine) avec un acide gras et une molécule de galactose. Retrouvé dans le tissus nerveux, hématies, leucocytes et spermatozoïdes Les cérébroglucosides : Glucose remplace galactose Les gangliosides : Cerveau et ganglions nerveux, renferme par ailleurs de l’acide neuraminique Les cérébrosulfatides : Dans ces structures, l’ose est porteur d’un groupement sulfaté Glucides BIOCHIMIE STRUCTURALE