Ghirlanda
- 1. Giovanni Ghirlanda Istituto di Patologia Medica Policlinico A.Gemelli Universita’ Cattolica del Sacro Cuore Roma Roma 23 giugno 2009 L’ asse entero insulare Nuove possibilità terapeutiche
- 2. Bayliss WM & Starling EH The mechanism of pancreatic secretion J. Physiol 28:325-335, 1902 1. Denervated jejunum releases pancreatic juice when acidified 2. SI extracts release pancreatic juice from denervated pancreas Blood-borne signal = secretin
- 3. DISCOVERY AND IDENTIFICATION OF GI TRACT PEPTIDES
- 4. LE INCRETINE Secretina GIP VIP PACAP Glucagone Peptidi glucagon-like GLP-1 GLP-2 glicentina oxintomodulina Stimolazione secrezione di insulina Azione trofica su cellule bersaglio Legame a recettori di membrana derivati dalla stessa famiglia AZIONI
- 5. DIFFERENTIAL PRE-TRANSLATIONAL PROCESSING OF PREPROGLUCAGON
- 6. GLP-1 e GIP sono sintetizzati e secreti dall’intestino dopo l’assunzione di cibo L-Cellule (ileo) Proglucagon GLP-1 [7–37] GLP-1 [7–36 NH 2 ] K-Cellule (digiuno) ProGIP GIP [1–42] GIP=glucose-dependent insulinotropic peptide; GLP-1=glucagon-like peptide-1 Drucker DJ. Diabetes Care. 2003; 26: 2929–2940.
- 7. > Insulina Fisiologia della digestione: Incretine GLP-1 GIP L K Ridotto Svuotamento gastrico < Glucagone < Produzione Epatica Glucosio > Uptake glucosio CNS < Assunzione di cibo Isole pancreatiche Tratto GI
- 8. Incretine: aumento della secrezione di insulina carico orale Time Plasma Insulin Carico iv Simile profilo glicemico Carico di glucosio IV od orale Plasma glucose IV oral “ Incretine” GLP-1 (7-36) GIP Altre incretine?
- 9. Meccanismo della secrezione insulinica insulina RE canali K ATP K + Ca 2 + GIP/GLP-1 PKA glucosio -cellula
- 10. Diminuito effetto Incretinico nel diabete tipo 2 0.6 0.5 0.4 0.3 0.2 0.1 0 80 60 40 20 0 80 60 40 20 0 Control Subjects (n=8) Type 2 Diabetic Patients (n=14) IR Insulin (mU / L) (mU / L) (nmol / L) (nmol / L) Time (min) Time (min) Adapted from Nauck M et. Diabetologia . 1986;29:46–52 180 60 120 0 0 60 120 180 ● ● Oral glucose load ○ ○ Intravenous glucose infusion Effetto Incretina 0.6 0.5 0.4 0.3 0.2 0.1 0
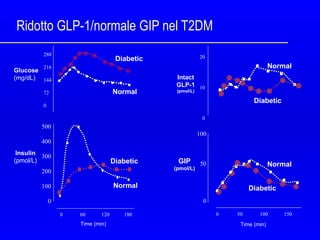
- 11. Ridotto GLP-1/normale GIP nel T2DM 20 10 0 Intact GLP-1 (pmol/L) Normal Diabetic 0 50 100 150 100 50 0 Time (min) GIP (pmol/L) Normal Diabetic Insulin (pmol/L) 0 60 120 180 500 400 300 200 100 0 Diabetic Normal 288 216 144 72 0 Glucose (mg/dL) Normal Diabetic Time (min)
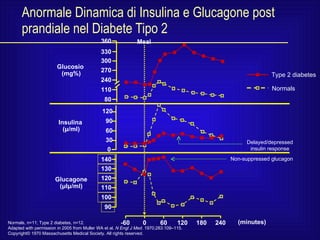
- 12. Anormale Dinamica di Insulina e Glucagone post prandiale nel Diabete Tipo 2 -60 0 60 120 180 240 360 330 300 270 240 110 80 120 90 60 30 0 Glucosio (mg%) Insulina ( μ /ml) Glucagone ( μ I μ /ml) Meal (minutes) Normals Delayed/depressed insulin response Non-suppressed glucagon Normals, n=11; Type 2 diabetes, n=12. Adapted with permission in 2005 from Muller WA et al. N Engl J Med . 1970;283:109–115. Copyright© 1970 Massachusetts Medical Society. All rights reserved. 140 130 120 110 100 90
- 13. Anormale Dinamica di Insulina e Glucagone post prandiale nel Diabete Tipo 2 -60 0 60 120 180 240 360 330 300 270 240 110 80 120 90 60 30 0 Glucosio (mg%) Insulina ( μ /ml) Glucagone ( μ I μ /ml) Meal (minutes) Type 2 diabetes Normals Delayed/depressed insulin response Non-suppressed glucagon Normals, n=11; Type 2 diabetes, n=12. Adapted with permission in 2005 from Muller WA et al. N Engl J Med . 1970;283:109–115. Copyright© 1970 Massachusetts Medical Society. All rights reserved. 140 130 120 110 100 90
- 14. Effetti dell’Infusione di GLP-1 su Insulina e Glucagone sono Dipendenti dal Glucosio Glucose Glucagon Once glucose levels fall, glucagon levels rebound Once glucose levels fall, insulin levels decline * P <0.05 Patients with Type 2 DM (N=10) mmol/L 15.0 12.5 10.0 7.5 5.0 250 200 150 100 50 mg/dL * * * * * * * pmol/L 250 200 150 100 50 40 30 20 10 0 mU/L * * * * * * * * Infusion Minutes pmol/L 20 15 10 5 0 60 120 180 240 * * * * pmol/L 20 15 10 5 Placebo GLP-1 Insulin 2.5 0 0 0 0 0 Adapted with permission from Nauck MA et al. Diabetologia . 1993;36:741–744. Copyright© 1993 Springer-Verlag.
- 15. L’inibizione della DPP-4 aumenta il GLP-1 attivo GLP-1 inattivo (>80% del pool) GLP-1 attivo Pasto DPP-4 Rilascio di GLP-1 intestinale GLP-1 t ½ =1–2 min Inibitore DPP-4 DPP-4=dipeptidil peptidasi-4; GLP-1=glucagon-like peptide-1 Adattato da Rothenberg P, et al. Diabetes. 2000; 49(suppl 1): A39. Abstract 160-OR. Adapted from Deacon CF, et al. Diabetes. 1995; 44: 1126-1131.
- 16. Incretine: potenziale intervento terapeutico GLP-1 Inattivo GIP Inattivo DPPIV Pasto Incretine GLP-1 GIP Altre incretine DPPIV Inhibitor GLP-1 or GLP-1 analogo GLP-1 Attivo 15 10 5 0 Meal DP-IV inibitore Placebo
- 17. Relazioni Anatomiche fra Cellule L GLP-1+ DPP-IV+ Endotelio
- 18. Incretine e Diabete Tipo 2 Inibitori della Dipeptidil Peptidasi -IV (DPP-IV) Farmaci a disposizione Sitagliptin Vildagliptin Farmaci in progresso Saxagliptin Alogliptin
- 19. Sitagliptin Monotherapy vs Placebo Effect on FBG over 24 weeks - All Patients Treated P< 0.001 both comparisons to placebo Treatment difference vs placebo Sita 100 mg = -17.1 mg/dL (-0.95 mmol/L) Sita 200 mg = -21.3 mg/dL (-0.1.18 mmol/L) N=234 N=247 N=244
- 20. Sitagliptin Monotherapy vs Placebo Reduction in post-meal glucose AUC Treatment difference vs placebo 100 mg = -65.6 ± 7.2 mg/dL 200 mg = -85.6 ± 7.1 mg/dL P<0.001 both comparisons vs pbo Solid= Baseline Dotted = Week 24 Placebo Sitagliptin 100mg Sitagliptin 200mg 0 60 120 0 60 120 0 60 120 180 252 216 144 288
- 21. Sitagliptin Monotherapy vs Placebo Effect on HbA 1c over 24 weeks - All Patients Treated Treatment difference vs placebo : Sitagliptin 100 mg = -0.79% P< 0.001 Sitagliptin 200 mg = -0.94% P< 0.001
- 22. Sitagliptin + Metformin vs Metformin alone Effect on FBG over 18 weeks - All Patients Treated -25.4 mg/dL (1.44 mmol/L) pbo-subtracted P< 0.001 vs placebo N=224 N=453
- 23. Sitagliptin + Metformin vs Metformin alone Effect on Reduction in post-meal glucose AUC AUC -81.5 (-104.2, -78.6) mg*hr/dL; p<0.001 0 60 120 0 60 120 Minutes after Initiation of Meal Sitaglitpin 100 mg + Metforminq.d. N=387 Metformin N=182 Baseline 24 weeks
- 24. Sitagliptin + Pio vs Pio alone Inclusion criteria HbA 1c 7 – 10%, p< 0.001 N=163 N=174 Effect on HbA1c over 24 weeks - All Patients Treated
- 25. Vildagliptin (LAF237) Reduces Meal-Related Glycemic Excursion in Subjects with Type 2 Diabetes Glucose Insulin GLP-1 Time (min) Time (min) Glucagon Ahren B, et al., J Clin Endocrinol Metab . 2004 May;89(5):2078-84
- 26. Vildagliptin Lowers HbA 1c Over the Course of 1 Year in Subjects with Type 2 Diabetes Adapted from Ahrén B, et al. Diabetes Care. 2004; 27(12):2874–2880. MET = metformin; PBO = placebo; ITT = intent to treat 6.8 7.2 7.6 8.0 8.4 – 4 0 4 8 12 16 20 24 28 32 36 40 44 48 52 Week Vildagliptin/MET (extension, ITT n = 42) PBO/MET (extension, ITT n = 29) Vildagliptin/MET (core, ITT n = 56) PBO/MET (core, ITT n = 51) HbA 1c (%) P < .0001 P < .0001 – 1.1 ± 0.2%
- 27. Funzione -Cellulare e Sensitbilità all’ Insulina dopo Vildagliptin vs Placebo in Pazienti con Diabete Tipo 2 Insulin Secretion Insulin Sensitivity Adaptation Index Patients on Stable Metformin Therapy *P < .05 vs placebo; † P < .01 vs placebo Adapted from Ahren B, et al. Diabetes Care . 2005;28:1936-1940. Vildagliptin/metformin Placebo/metformin 14 12 10 8 6 0 12 24 52 Time (wk) 0 12 24 52 Time (wk) 0.050 0.045 0.040 0.035 0.030 0.025 pmol/L 30min/(mmol/L) 0 12 24 52 Time (wk) 300 275 250 225 200 * * mL · min -1 · m -2 * * * * * †
- 28. Incretine e Diabete Tipo 2 Farmaci a disposizione Incretinomimetici Analoghi del GLP-1
- 29. Incretine e Diabete Tipo 2 Incretinomimetici Analoghi del GLP-1 Liraglutide (NN2211) -GLP-1 acilato, si lega all’albumina con: -ridotta degradazione da parte della DPP-IV -ritardato e prolungato assorbimento dal sito di iniezione -ridotta clearance renale
- 30. Acilazione del GLP-1 comporta Resistenza alla DPPIV Ridotta eliminazione renale GLP-1 è rapidamente degradato dalla DPPIV GLP-1 (7-37) AtTIVo Glu Gly Thr Phe Thr Ser Asp Lys Ala Ala Gln Gly Glu Leu Tyr Ser Ile Ala Trp Leu Val Lys Gly Arg Gly Val Ser Glu Phe GLP-1 (9-37) INAtTIVo DPPIV Liraglutide (NN2211) His Ala Glu Gly Thr Phe Thr Ser Asp Lys Ala Ala Gln Gly Glu Leu Tyr Ser Ile Ala Trp Leu Val Lys Gly Arg Gly Val Ser Glu Phe His Ala Glu Gly Thr Phe Thr Ser Asp Lys Ala Ala Gln Gly Glu Leu Tyr Ser Ile Ala Trp Leu Val Arg Gly Arg Gly Val Ser Glu Phe His Ala Glu Gly Thr Phe Thr Ser Asp Lys Ala Ala Gln Gly Glu Leu Tyr Ser Ile Ala Trp Leu Val Arg Gly Arg Gly Val Ser Glu Phe palmitoil Glu
- 31. Incretine e Diabete Tipo 2 Incretinomimetici Agonisti del GLP-1 Exenatide (Exendin 4, LY2148568) -Estratto dalla saliva di una lucertola del deserto (Gila Monster o Heloderma suspectum) -Presenta una elevata omologia con il GLP-1 umano -Resistente alla degradazione, lunga emivita -Si lega agli stessi recettori del GLP-1 umano
- 32. Exendina-4 e GLP-1 Exendin-4 ha parziale omologia aminoacidica GLP-1. Exendin-4 e GLP-1 si legano ai recettori pancreatici del GLP-1 in vitro . Amino Acid Sequences:
- 33. Incretine e Diabete Tipo 2 Incretinomimetici Agonisti del GLP-1(Exenatide) Numerosi studi in corso nei diabetici tipo 2 hanno documentato che questo farmaco: aumenta sia la prima che la seconda fase della secrezione insulinica con un andamento simile a quello dei soggetti normali produce una significativa riduzione della HbA1c produce una progressiva riduzione del peso corporeo riduce i livelli di glucosio a digiuno e post-prandiali migliora la funzione beta-cellulare
- 34. Liraglutide Derivato acilato del GLP-1 con lunga durata d’azione (emivita: 11-13 ore) Si autoassocia e si lega ai siti di legame per gli acidi grassi delle albumine plasmatiche L’albumina agisce come un reservoir per assicurare il legame del liraglutide al sito attivo Questo legame causa un profilo farmacocinetico che rallenta l’assorbimento e allunga l’emivita Monosomministrazione giornaliera
- 35. Effetti degli Incretino-mimetici Riduzione della glicemia a digiuno Riduzione della glicemia post-prandiale Miglioramento del compenso metabolico (HbA 1c ) Riduzione del peso corporeo Miglioramento dei fattori di rischio CV (?) “ Protezione” β -cellule (?) Qual è l’efficacia degli incretino-mimetici ?
- 36. Exenatide riduce l’HbA 1c dopo 30 settimane Popolazione ITT; Media (SE); MET (N = 336), SFU (N = 377), MET + SFU (N = 733); *P <.005 vs placebo. Basale medio HbA 1c da 8.2% a 8.7% a seconda dei gruppi dello studio. DeFronzo RA, et al. Diabetes Care 28:1092-1100, 2005; B use JB, et al. Diabetes Care 27:2628-2635, 2004; Kendall DM, et al. Diabetes Care 28:1083-1091, 2005 SFU (n=123) MET + SFU (n=247) MET (n=113) Variazioni HbA 1c (%) Placebo BID Exenatide 5 µg BID Exenatide 10 µg BID * 0.2 -0.6 * -0.8 0.1 -0.5 * -0.9 -0.4 * -0.8 * -1 -0.5 0 0.5 0.1 *
- 37. Estensione Open-Label - Exenatide mantiene la riduzione di HbA 1c per 156 settimane Klonoff DC et al. Curr Med Res 24:275-286, 2008 Basale 8.2 + 0.1% 156° settimana -1.0% (95% CI: da -1.1 a -0.8%) Trattamento (settimane) Qual è l’efficacia degli incretino-mimetici ?
- 38. Estensione Open-Label - Exenatide riduce progressivamente il peso corporeo in 156 settimane Klonoff DC et al. Curr Med Res 24:275-286, 2008 Basale 99.3 + 1.2 kg 156° settimana -5.3 kg (95% CI: da -6.0 a -4.5 kg Trattamento (settimane) Variazione peso corporeo dal basale (kg) Qual è l’efficacia degli incretino-mimetici ?
- 39. Effetti della somministrazione settimanale di una formulazione di exenatide a lungo rilascio (LAR) sul controllo metabolico e sul peso in soggetti con DMT2 Kim D. et al. Diabetes Care 30:1487–1493, 2007 Effetto dell’exenatide LAR su HbA 1c Effetto dell’exenatide LAR su BMI Qual è l’efficacia degli incretino-mimetici ? Tempo (settimane) Tempo (settimane) Media ( SE) A1C (%) Variazione Media ( SE) ponderale (kg) Δ Media: Δ Media:
- 40. Estensione Open-Label - Riduzione dei fattori di rischio cardiovascolare dopo 3.5 anni di trattamento con exenatide (n = 151) Klonoff DC et al. Curr Med Res 24:275-286, 2008 Fattore di rischio cardiovascolare Basale (media + SEM) Variazione rispetto al basale (media + SEM) Media Variazione % Valore di p Trigliceridi (mg/dl) Colesterolo totale (mg/dl) Colesterolo HDL (mg/dl) Colesterolo LDL (mg/dl) Pressione arteriosa sistolica (mmHg) Pressione arteriosa diastolica (mmHg) Qual è l’efficacia degli incretino-mimetici ?
- 41. Liraglutide induce una riduzione continua del peso corporeo fino a 3 kg Vilsbøll T et al, Diabetes Care 30: 1608-1610, 2007 Qual è l’efficacia degli incretino-mimetici ? Tempo (settimane) 14° Settimana: 1.2 kg 1.90 mg/die versus placebo ( p <0.039) – 3 – 2 – 1 0 Perdita di peso dal basale (kg) 0.65 mg/die 1.25 mg/die 1.90 mg/die Placebo Valori medi 0 2 4 6 8 10 12 14
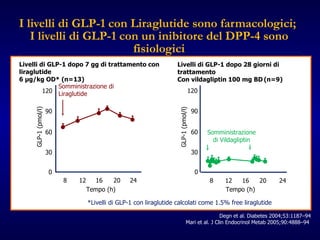
- 42. I livelli di GLP-1 con Liraglutide sono farmacologici; I livelli di GLP-1 con un inibitore del DPP-4 sono fisiologici Degn et al. Diabetes 2004;53:1187–94 Mari et al. J Clin Endocrinol Metab 2005;90:4888–94 Tempo (h) 30 60 90 120 8 16 12 20 24 0 GLP-1 (pmol/l) Tempo (h) 30 60 90 120 8 16 12 20 24 0 GLP-1 (pmol/l) Somministrazione di Liraglutide Livelli di GLP-1 dopo 7 gg di trattamento con liraglutide 6 µg/kg OD* (n=13) Livelli di GLP-1 dopo 28 giorni di trattamento Con vildagliptin 100 mg BD (n=9) Somministrazione di Vildagliptin *Livelli di GLP-1 con liraglutide calcolati come 1.5% free liraglutide
- 43. Exenatide (Exendina-4) rimane in circolo più a lungo del GLP-1 Tempo dopo bolo SC (ore) Media Log (SE) GLP-1 plasmatico (pM) Tempo dopo bolo SC (ore) Media Log (SE) Exendina-4 plasmatica (pM) Exendina-4 GLP-1 0 1 2 3 4 5 6 10 10 100 1000 10000 100000 0 1 2 3 4 5 6 10 10 100 1000 10000 100000 Parkes D, et al. Drug Dev Res. 2001;53:260-267 N = 4-7 (ratti); p<0.05 50 nmol 5 nmol 0.5 nmol
- 44. GLP-1 + GIP Sì GLP-1 No Inibitori del DPP-4 Agonisti GLP-1R Meccanismo d’azione Attivazione del sensore del portale del glucosio Agonisti del Recettore GLP-1 vs Inibitori DPP-4 + ++ Secrezione Insulina ++ ++ Secrezione Glucagone ± inibito Svuotamento gastrico No Sì Perdita di peso Espansione massa β -cellulare Sì Sì No Sì Nausea e vomito No Sì Potenziale immunogenicità fisiologica farmacologica Concentrazione di GLP-1 Orale Iniezione Somministrazione
- 45. Gli incretino-mimetici e gli inibitori del DPP-4 sono simili dal punto di vista terapeutico ? Riduzione di HbA 1c lievemente superiore con Exenatide rispetto a quanto osservato con farmaci inibitori del DPP-4 , seppure con un certo grado di sovrapposizione (Exenatide: 0,8-1,2% vs inibitori del DPP-4: 0,6-1,0%). Chiare differenze riguardo all’effetto di riduzione del peso corporeo (maggiore con Exenatide e Liraglutide rispetto a quanto osservato con inibitori del DPP-4). Messaggi Chiave
- 46. In quali pazienti e quando intraprendere la terapia basata sulle Incretine?
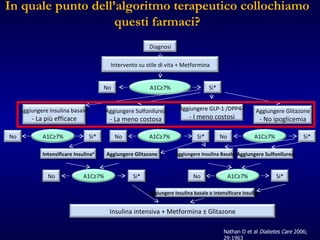
- 47. In quale punto dell’algoritmo terapeutico collochiamo questi farmaci? Nathan D et al Diabetes Care 2006; 29:1963 Diagnosi Intervento su stile di vita + Metformina No Si* A1C ≥7% No Si* A1C≥7% No Si* A1C≥7% No Si* A1C≥7% Aggiungere Insulina basale # - La più efficace Aggiungere Sulfonilurea - La meno costosa Aggiungere Glitazone - No ipoglicemia Intensificare Insulina # Aggiungere Glitazone Aggiungere Insulina Basale # Aggiungere Sulfonilurea Aggiungere Insulina basale o intensificare insulina # Insulina intensiva + Metformina ± Glitazone No Si* No Si* A1C≥7% A1C≥7% Aggiungere GLP-1 /DPP4-I - I meno costosi
- 48. Pazienti con DMT2 che assumono metformina, sulfonilurea, o una combinazione di metformina e una sulfonilrea ma che non hanno ancora ottenuto un adeguato controllo glicemico . Pazienti con DMT2 sovrappeso/Obesi : effetti favorevoli o neutri sul peso corporeo. Anziani: bassa incidenza di ipoglicemia, sicuri e ben tollerati, migliorano il controllo glicemico anche in monoterapia. Terapia con Incretine nel DMT2 : in quali pazienti ?
- 49. … “ L’esperienza sulla terapia con inhibitori del DPP-4 in pazienti con insufficienza cardiaca congestizia di classe funzionale I-II secondo la New York Heart Association (NYHA) è limitata e quindi devono essere usati con prudenza in questi pazienti. Non c’è esperienza sull’uso degli inibitori del DPP-4 in studi clinici in pazienti con classe funzionale NYHA III-IV e quindi non è raccomandato l’uso in questi pazienti .”… POTENZIALMENTE INDICATI IN : Terapia con Incretine nel DMT2 : in quali pazienti ? Pazienti con patologie cardiovascolari : no edema, effetti favorevoli o neutri sul profilo lipidico e sulla pressione arteriosa.
- 50. In quali pazienti e quando intraprendere la terapia basata sulle Incretine ? Nelle attuali Linee Guida Internazionali , i farmaci che agiscono sull’asse delle incretine non hanno una collocazione ufficiale. È possibile ipotizzare un loro impiego ottimale in pazienti diabetici che non raggiungono l’obiettivo terapeutico (HbA 1c >7.0%) in associazione con metformina, sulfonilurea, o con combinazione di metformina e sulfonilurea; nei pazienti in sovrappeso; negli anziani. Messaggi Chiave
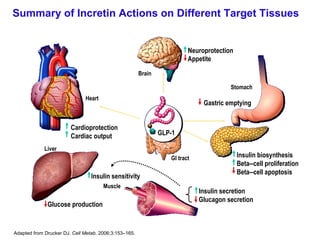
- 51. Summary of Incretin Actions on Different Target Tissues Adapted from Drucker DJ. Cell Metab . 2006;3:153–165. Insulin secretion Glucagon secretion Gastric emptying Appetite Cardioprotection Cardiac output Insulin biosynthesis Beta – cell proliferation Beta – cell apoptosis Neuroprotection Glucose production Insulin sensitivity Brain Heart GI tract Liver Muscle Stomach GLP-1
- 52. L’esperienza di un anno nei Centri Diabetologici Italiani Prof Giovanni Ghirlanda Servizio di Diabetologia Dipartimento di Medicina Interna Policlinico A. Gemelli Università Cattolica Roma
- 53. EXENATIDE * * p<0,001 vs Baseline
- 54. EXENATIDE * p<0,001 vs Baseline *
- 55. EXENATIDE * * p<0,008 vs Baseline
- 56. EXENATIDE * * p<0,001 vs Baseline
- 57. INIBITORI DELLA DPP-4 * * p<0,001 vs Baseline
- 60. INIBITORI DELLA DPP-4 * * p<0,001 vs Baseline
- 61. Nel gruppo trattato con Byetta ci sono stati due pazienti che hanno interrotto il trattamento per un rialzo asintomatico delle amilasi, con un rapido ritorno alla normalità dopo la sospensione del farmaco. Nel gruppo trattato con gli inibitori c’è stato un caso di interruzione del trattamento per la comparsa di intensa astenia dopo la somministrazione del farmaco
Editor's Notes
- #18: DPP-IV is a widely expressed enzyme produced in many different cell types. DPP-IV exists as 2 principal forms, a soluble form that circulates in the plasma not directly associated with specific cell types, and a membrane anchored form directly tethered to cell membranes. DPP-IV+ endothelial cells are anatomically located in close approximation to the enteroendocrine L cells that synthesize GLP-1.
- #26: This slide illustrates the results of a 4-week, placebo-controlled trial of the DPP-4 inhibitor, LAF237 (Vildagliptin) in patients with type 2 diabetes. Drug-naïve, diet-treated patients (baseline HbA 1c ~7.2%) were randomized to receive placebo or LAF237 (100 mg) once daily. Depicted here are the plasma levels of glucose, insulin, active GLP-1, and glucagon measured during a standardized meal challenge performed on day 28 of treatment. Fasting and postprandial glucose levels were significantly decreased in patients receiving LAF237, as was the glucagon response to the mixed meal. Plasma levels of intact (N-terminally detected) GLP-1 were significantly increased. The insulin response to the meal was unchanged; however, the insulinogenic index (ratio of insulin to glucose) was increased, suggesting relative stimulation of insulin secretion.
- #27: This slide illustrates the results of a 12-week multicenter, randomized, double-blind placebo-controlled study and a subsequent 40-week open label extension study (total of 52 weeks) comparing the effects of treatment with vildagliptin (n = 56) versus placebo (n = 51) when added to a stable metformin regimen (1500-3000 mg/d) in the treatment of 107 patients with T2DM. HbA 1c levels were decreased at 12 weeks in the vildagliptin group (–0.6 ± 0.1%) but not in the placebo group (0.1 ± 0.1%), with a between-group difference in the adjusted mean change of –0.7±0.1% ( P < .0001) in favor of vildagliptin. In the 52-week extension group, HbA 1c increased among placebo-treated patients remaining on metformin at a rate of 0.0656% per month but decreased in the vildagliptin-treatment group, for a between-group difference at end point of –1.1 ± 0.2% ( P < .0001). At the study end point, 41.7% of patients in the vildagliptin group had achieved HbA 1c < 7.0% compared with only 10.7% of those taking placebo plus metformin.
- #28: This slide illustrates the results of a multicenter, randomized, double-blind, placebo-controlled study comparing the effects of 52 weeks of treatment with vildagliptin 50 mg/day (n=31) versus placebo (n=26) administered to patients with T2DM who continued on a stable dosage of metformin (1,500-3,000 mg/d). The slide shows (1) insulin secretion, (2) insulin sensitivity, and (3) the adaptation index following a standardized 465-kcal breakfast meal, as measured at baseline and after 12, 24, and 52 weeks of vildagliptin treatment. In the vildagliptin-treated group, insulin secretion was significantly augmented in comparison to the placebo group. This effect continued over the entire 52-week period, indicating that vildagliptin improves β- cell function in a sustained manner. Similarly, insulin sensitivity significantly improved among vildagliptin vs placebo-treated patients. The significant increase in adaptation index (the product of insulin sensitivity and secretion) in the vildagliptin group suggests that the drug improves β- cell function independent from changes in insulin sensitivity.
- #52: Summary of Incretin Actions on Different Target Tissues 1,2 The 2 principal incretins, GIP and GLP-1, both act on the beta cell to stimulate glucose-dependent insulin secretion, and in preclinical studies both incretins stimulate beta-cell proliferation and reduce beta-cell apoptosis. GLP-1 also has multiple actions on other cell types, including suppression of glucagon secretion from the islet alpha cell, inhibition of food intake and gastric emptying, and regulation of cardiovascular function and contractility. Although GLP-1 action on the liver and muscle is thought to be indirect, possibly via other hormones or through the nervous system, treatment of subjects with diabetes with GLP-1 receptor (GLP-1R) agonists has also been associated with increased insulin sensitivity in peripheral tissues such as muscle and liver. References: 1. Drucker DJ. Biological actions and therapeutic potential of the proglucagon-derived peptides. Nat Clin Prac Endocrinol Metab. 2005;1:22–31. 2. Drucker DJ. The biology of incretin hormones. Cell Metab. 2006;3:153 – 165.






![GLP-1 e GIP sono sintetizzati e secreti dall’intestino dopo l’assunzione di cibo L-Cellule (ileo) Proglucagon GLP-1 [7–37] GLP-1 [7–36 NH 2 ] K-Cellule (digiuno) ProGIP GIP [1–42] GIP=glucose-dependent insulinotropic peptide; GLP-1=glucagon-like peptide-1 Drucker DJ. Diabetes Care. 2003; 26: 2929–2940.](https://image.slidesharecdn.com/ghirlanda-100212161649-phpapp02/85/Ghirlanda-6-320.jpg)