Olla de-presion
- 1. TERMODINÁMICA 1 OLLA A PRESIÓN 1.- OBJETIVOS: Determinar la presión atmosférica en sucre por varios métodos. 1.-Tablas Métodos 2.-Ecuaciones de presión de vapor 3.-Principio de estados correspondientes Comparar la presión atmosférica calculada con el dato de SENHAMI. Aplicar el balance de energía a una olla a presión. Elaborar el perfil de temperatura tiempo y presión del proceso. Determinar la masa final del agua que queda en la olla en forma experimental y teórico. Calcular el porcentaje de error. 2.- FUNDAMENTO TEÓRICO: La olla a presión es un recipiente hermético para cocinar que no permite la salida de aire o líquido por debajo de una presión establecida. Debido a que el punto de ebullición del agua aumenta cuando se incrementa la presión, la presión dentro de la olla permite subir la temperatura de ebullición por encima de 100 °C (212 °F), en concreto hasta unos 130 °C. La temperatura más alta hace que los alimentos se cocinen más rápidamente llegando a reducir los tiempos de cocción tradicionales entre tres o cuatro veces. Por ejemplo,un repollo se cocina en un minuto, las judías verdes en cinco,las patatas pequeñas y medianas (hasta 200 g) pueden tardar unos cinco minutos y un pollo completo no más de veinticinco a treinta minutos. Generalmente, se utiliza para conseguir en un corto período los mismos efectos del estofado o de la cocción a fuego lento. Una válvula libera el vapor cuando la presión llega al límite establecido; normalmente, la presión levanta un tope permitiendo que el vapor escape. Existe una válvula de seguridad regulada a una presión superior a la de funcionamiento. Si la temperatura interna (y por tanto, la presión) es demasiado alta, funcionaría esta válvula, dejando escapar la presión. No es raro que ocurra puesto que ciertos alimentos tienen hojas que pueden obstruir el orificio de salida de la válvula de funcionamiento. Las modernas ollas a presión se fabrican normalmente en aluminio o acero inoxidable. Termómetro Termómetro clínico digital.
- 2. termodinamica TERMODINÁMICA 2 Un termógrafo, este aparato es capaz de medir y registrar las variaciones de temperatura. El termómetro (del griegoθερμός (thermos), el cuál significa "caliente" y metro, "medir") es un instrumento de medición de temperatura. Desde su invención ha evolucionado mucho, principalmente a partir del desarrollo de los termómetros electrónicos digitales. Inicialmente se fabricaron aprovechando el fenómeno de la dilatación, por lo que se prefería el uso de materiales con elevado coeficiente de dilatación, de modo que, al aumentar la temperatura, su estiramiento era fácilmente visible. El metal base que se utilizaba en este tipo de termómetros ha sido el mercurio, encerrado en un tubo de vidrio que incorporaba una escala graduada. El creador del primer termoscopio fue Galileo Galilei; éste podría considerarse el predecesor del termómetro. Consistía en un tubo de vidrio terminado en una esfera cerrada; el extremo abierto se sumergía boca abajo dentro de una mezcla de alcohol y agua, mientras la esfera quedaba en la parte superior. Al calentar el líquido, éste subía por el tubo. La incorporación, entre 1611 y 1613, de una escala numérica al instrumento de Galileo se atribuye tanto a Francesco Sagredo1 como a Santorio,2 aunque es aceptada la autoría de éste último en la aparición del termómetro. En España se prohibió la fabricación de termómetros de mercurio en julio de 2007, por su efecto contaminante. En América latina, los termómetros de mercurio siguen siendo ampliamente utilizados por la población. No así en hospitales y centros de salud donde por regla general se utilizan termómetros digitales Manómetro El manómetro (del gr. μανός, ligero y μέτρον, medida) es un instrumento de medición para la presión de fluidos contenidos en recipientes cerrados. Se distinguen dos tipos de manómetros, según se empleen para medir la presión de líquidos o de gases.1
- 3. TERMODINÁMICA 3 Multímetro Polímetro analógico y polímetro digital Pirómetro Un pirómetro, dispositivo capaz de medir la temperatura de una sustancia sin necesidad de estar en contacto con ella. El término se suele aplicar a aquellos instrumentos capaces de medir temperaturas superiores a los 600 grados celsius. El rango de temperatura de un pirómetro se encuentra entre -50 grados celsius hasta +4000 grados celsius. Una aplicación típica es la medida de la temperatura de metales incandescentes en molinos de acero o fundiciones.
- 4. termodinamica TERMODINÁMICA 4 Termopar Un termopar (también llamado termocupla) es un transductor formado por la unión de dos metales distintos que produce una diferencia de potencial muy pequeña (del orden de los milivoltios) que es función de la diferencia de temperatura entre uno de los extremos denominado «punto caliente» o «unión caliente» o de «medida» y el otro llamado «punto frío» o «unión fría» o de «referencia» (efecto Seebeck). Normalmente las termocuplas industriales estan compuestas por una vaina, que no es más que un tubo de acero inoxidable u otro material. En un extremo de esa vaina está la unión, y en el otro el terminal eléctrico de los cables, protegido dentro de una caja redonda de aluminio (cabezal). En Instrumentación industrial, los termopares son usados como sensores de temperatura. Son económicos, intercambiables, tienen conectores estándar y son capaces de medir un amplio rango de temperaturas. Su principal limitación está en la exactitud, pues es fácil obtener errores del sistema cuando se trabaja con temperaturas inferiores a un grado Celsius. El grupo de termopares conectados en serie recibe el nombre de termopila. Tanto los termopares como las termopilas son muy usados en aplicaciones de calefacción a gas. Potencia En física, potencia (símbolo P)nota 1 es la cantidad de trabajo efectuado por unidad de tiempo. Si W es la cantidad de trabajo realizado durante un intervalo de tiempo de duración Δt, la potencia media durante ese intervalo está dada por la relación:
- 5. TERMODINÁMICA 5 Potencia mecánica La potencia mecánica aplicada sobre un sólido rígido viene dado por el producto de la fuerza resultante aplicada por la velocidad: Si además existe rotación del sólido y las fuerzas aplicadas están cambiando su velocidad angular: Donde: , son la fuerza resultante y el momento resultante. , son la velocidad del punto donde se ha calculado la resultante efectiva y la velocidad angular del sólido. Para un sólido deformable o un medio continuo general la expresión es más compleja y se expresa como producto del tensor tensión y el campo de velocidades. la variación de energía cinética viene dada por: Donde: , son las componentes del tensor de tensiones de Cauchy. , son las componentes del tensor de velocidad de deformación. Potencia eléctrica Artículo principal: Potencia eléctrica La potencia eléctrica P desarrollada en un cierto instante por un dispositivo viene dada por la expresión Donde: P(t) es la potencia instantánea, medida en vatios (julios/segundos). I(t) es la corriente que circula por él, medida en amperios. V(t) es la diferencia de potencial (caída de voltaje) a través del componente, medida en voltios. Si el componente es una resistencia, tenemos:
- 6. termodinamica TERMODINÁMICA 6 Dónde: R es la resistencia, medida en ohmios. 3.-MATERIALES Y EQUIPOS: Olla a presión Termómetro de vidrio Termocupla Manómetro multímetro Estufa eléctrica Densímetro digital Vaso de precipitado Agua 4.-PROSEDIMIENTO DE LA PRÁCTICA: a) Utilizar un multímetro, determinar la potencia de la hornilla eléctrica. b) Con una muestra de 60 ml de agua determinar la temperatura de ebullición utilizando un termómetro de vidrio y termocupla. c) Se dispone una olla a presión con una capacidad de 6.75 litros a la que se añade un litro de agua potable. d) Se suministra calor mediante la hornilla hasta alcanzar la presión de operación de la olla y a partir de ese momento controlar 15 minutos. e) Concluido el proceso medir la cantidad de agua que a quedado en la olla. f) Los datos para el cálculo de la presión atmosférica se hacen en un volumen de 50ml de agua. 5.- TABULACIÓN DE DATOS: R(Ω) V(voltios) ῥ(gr/ml) Ti(˚C) Teb(Termómetro) T(termocupla) P.atmosferica(sanhami) 51.3 217 .9973 21.1 90 90.1 726.2 milibares Tiempo (min) Temperatura (°C) Presion (psi) Temp. Sup(°C) Temperatura de ebullición (°K) 0 0 0 0 364.85 3 24 1 28 6 32 1 29 9 46.7 1.1 29.5 12 63.7 1.6 31.5 15 81.6 4 33.5
- 7. TERMODINÁMICA 7 6.- CALCULOS: Determinación de Patm por tablas T1=115.40C= 388.55°K Psat=171.452Kpa Psenhami=72.08Kpa Pman=13.6Psi=93.7687Kpa Patm=Pabs˗Pman Patm=(171.452˗93.7687)Kpa Patm=77.68Kpa Determinación de Patm por Ec.presión de vapor Propiedades del agua (H2O) Ecuación de vapor TC (K) PC (KPa) VPA VPB VPC VPD HENDRICK 647.3 22120 -7.7645 1.45838 -2.77580 -1.23303 HARLACHER 647.3 22120 -7.7645 1.45838 -2.77580 -1.23303 ANTOINE 647.3 22120 -7.7645 1.45838 -2.77580 -1.23303 1. Ec. Hendricks Ln (Psat/Pc)=(1-X)˗1*(AX+BX1.5+CX3+DX6) X=1-Tsat/Tc Psat= Patm = 74.803Kpa A=-7.7645 B=1.45838 18 91.7 9.1 39.5 21 112.5 13.5 41.5 24 115.3 13.6 43.5 27 115.4 13.6 44 30 115.4 13.6 44 33 115.4 13.6 44.5 36 115.5 13.6 44.5
- 8. termodinamica TERMODINÁMICA 8 C=-2.7758 D=-1.23303 Tc = 647.3 K Pc = 22120 Kpa w = 0.235 2. Ec. Harlacher Ln (Psat) = (A+B) / (T+CXln (T)+DX(Psat/T2)) Psat = 3.26 Kpa 3. Ec. Antoine Ln (Psat) = (A-B)/(T+C) Psat = 0.0423Kpa Ec. Frost-Kalkwarf-Thodos Ln (Psat) = A- (B/T) +ClnT+(DlnPsat/T2) Psat = 2.7531E-11 Kpa Calculo De Patm Por P.E.C TI = 364.85 K Tr = 364.85 𝐾 647 .3 𝐾 = 0.56 Tc = 647.3 K Zliq, sat = 0.033 Pc = 22120 Kpa Zvap, sat = 0.97 Pr = 0.027 𝑃𝑟 = 𝑃 𝑃𝑐 𝑃𝑠𝑎𝑡 = 𝑃𝑟 ∗ 𝑃𝑐 = 0.027* 22120 Kpa Psat = 597.24 Kpa Patm = (597.24-93.7687) Kpa Patm = 503.47Kpa Comparar la presión atmosférica con el dato de SENHAMI Por tablas Patm =77.68 Kpa Psenhami=72.08Kpa
- 9. TERMODINÁMICA 9 Por Ec.presión de vapor Patm = 74.803 Kpa Psenhami=72.08Kpa Sistema: olla • Abierto • Bordes fijos, W = 0 Ec = 0 Ep = 0 Balance de materia: 𝑚 𝑒𝑛𝑡 − 𝑚 𝑠𝑎𝑙 = 𝑑𝑚 𝑑𝑡 𝑚 𝑒𝑛𝑡 = 0 −𝑚 𝑠𝑎𝑙 = 𝑚 𝑓 − 𝑚 𝐼 Ec.1 Balance de energía: −𝑚 𝑠𝑎𝑙 𝐻𝑠𝑎𝑙 + 𝑄 = 𝑑(𝑈𝑚) 𝑑𝑡 −𝐻𝑠𝑎𝑙 𝑚 𝑠𝑎𝑙 + 𝑄 = 𝑈𝑓 𝑚 𝑓 − 𝑈𝐼 𝑚 𝐼 Ec.2 Reemplazar ec.1, en ec.2 −𝐻𝑠𝑎𝑙(𝑚 𝑓 − 𝑚 𝐼) + 𝑄 = 𝑈𝑓 𝑚 𝑓 − 𝑈𝐼 𝑚 𝐼 Ec.A Calculo del calor transferido. 𝑃 = 𝑉2 𝑅 = 2172 51.3 = 917.91 𝑊𝑎𝑡𝑡𝑠 𝑄 = 917.91 𝐽 𝑠𝑒𝑔 ∗ 1 𝐾𝐽 1000 𝐽 ∗ 20.31 𝑚𝑖𝑛 ∗ 60 𝑠𝑒𝑔 1 𝑚𝑖𝑛 = 1118.56 𝐾𝐽 P = ctte Hsal = ctte T = ctte Condiciones iniciales: VT = 6.75 Lt. = 0.00675 m3 Vagua = 750 ml = 0.0008 m3 TI = 115.40C = 388.55 K a tablas leer PI = 171.452Kpa Entonces es mezcla líquido vapor Vliq. sat = 0.0011m3/Kg Vvap. sat= 1.025 m3/Kg Uliq. sat = 483.976 KJ/Kg Uvap. sat = 2524.16 KJ/Kg
- 10. termodinamica TERMODINÁMICA 10 Hvap. sat = Hsal = 2699.54 KJ/Kg Calculo masa inicial. ῥ = 𝑚 𝑉 Entonces 𝑚 𝐼 = 0.0008 𝑚3 ∗ 997.3 𝐾𝑔 𝑚3 mI = 0.7978 Kg Calculo volumen específico inicial. 𝑉𝐼 = 𝑉𝑇 𝑚 𝐼 = 0.00675 𝑚3 0.7978 𝐾𝑔 = 8.4607𝐸 − 3 𝑚3 𝐾𝑔 Calculo de calidad inicial. 𝑉𝐼 = 𝑉𝑣𝑎𝑝. 𝑠𝑎𝑡 𝑋𝐼 + (1 − 𝑋𝐼)𝑉𝑙𝑖𝑞.𝑠𝑎𝑡 8.4607𝐸 − 3 = 1.025 𝑋𝐼 + (1 − 𝑋𝐼) 0.0011 XI = 0.00719 𝑈𝐼 = 𝑈𝑣𝑎𝑝. 𝑠𝑎𝑡 𝑋𝐼 + (1 − 𝑋𝐼)𝑈𝑙𝑖𝑞.𝑠𝑎𝑡 𝑈𝐼 = 2524.16 ∗ 0.00719 + (1 − 0.00719)∗483.976 UI = KJ/Kg Condiciones finales VF = 520 ml = 0.00052 m3 ῥ = 𝑚 𝑉 Entonces 𝑚 𝐹 = 0.00052 𝑚3 ∗ 997.3 𝐾𝑔 𝑚3 mF = 0.5186Kg entonces mF, teórico −𝐻𝑠𝑎𝑙(𝑚 𝑓 − 𝑚 𝐼) + 𝑄 = 𝑈𝑓 𝑚 𝑓 − 𝑈𝐼 𝑚 𝐼 Ec. A 𝑉𝐹 = 𝑉 𝑇 𝑚 𝐹 = 𝑉𝑣𝑎𝑝. 𝑠𝑎𝑡 𝑋 𝐹 + (1 − 𝑋 𝐹)𝑉𝑙𝑖𝑞.𝑠𝑎𝑡 0.0015 = 1.025𝑋 𝐹 + (1 − 𝑋 𝐹) ∗ 0.0011 Ec. B 𝑈 𝐹 = 𝑈𝑣𝑎𝑝. 𝑠𝑎𝑡 𝑋 𝐹 + (1 − 𝑋 𝐹)𝑈𝑙𝑖𝑞.𝑠𝑎𝑡 𝑈 𝐹 = 2524.16 ∗3.9E-4+(1 −3.9E-4)483.976 Ec. C Resolver 3 ecuaciones con 3 incógnitas.
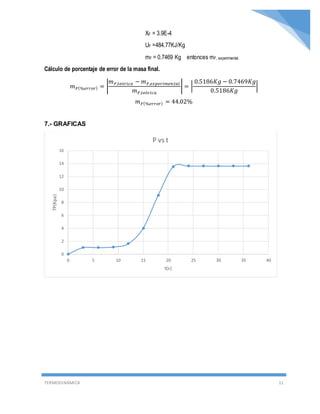
- 11. TERMODINÁMICA 11 XF = 3.9E-4 UF =484.77KJ/Kg mF = 0.7469 Kg entonces mF, experimental Cálculo de porcentaje de error de la masa final. 𝑚 𝐹(%𝑒𝑟𝑟𝑜𝑟) = | 𝑚 𝐹,𝑡𝑒ó𝑟𝑖𝑐𝑎 − 𝑚 𝐹,𝑒𝑥𝑝𝑒𝑟𝑖𝑚𝑒𝑛𝑡𝑎𝑙 𝑚 𝐹,𝑡𝑒ó𝑟𝑖𝑐𝑎 | = | 0.5186𝐾𝑔 − 0.7469𝐾𝑔 0.5186𝐾𝑔 | 𝑚 𝐹(%𝑒𝑟𝑟𝑜𝑟) = 44.02% 7.- GRAFICAS 0 2 4 6 8 10 12 14 16 0 5 10 15 20 25 30 35 40 TP(Kpa) t(s) P vs t
- 12. termodinamica TERMODINÁMICA 12 8.- CONCLUSIONES: La práctica se realizó con normalidad, los datos que se obtuvieron de la presión y temperatura de la olla de presión estaba bien, la presión que se calculó experimentalmente se comparó con la presión obtenida por senhami y se pudo comprobar que daban casi el mismo valor. Pero para el cálculo de la presión de saturación solo se realizó con la primera ecuación de vapor porque con las demás no se puede determinar ya que sale datos incoherentes. Para el cálculo de la masa final del agua se obtuvo un error del 44.02%, esto se pudo deber a errores durante la toma de datos. 9.- BIBLIOGARFIA: http://es.wikipedia.org/wiki/Mult%C3%ADmetro http://es.wikihow.com/usar-una-olla-de-presi%C3%B3n http://www.fluke.com/fluke/eses/products/termometros.htm GOMEZ-NIETO, M. and G. THODOS: Ind. Eng. Chem. Fund., Vol. 17, p.45 (1978). 0 5 10 15 20 25 30 35 40 T(°C) t(s) T vs t