11. ormonodipendenza ca prostata
- 1. Ormonodipendenza dei tumori prostatici Prof.ssa Elisa Petrangeli 28 marzo 2011
- 2. MECCANISMI MOLECOLARI E CELLULARI DELLO SVILUPPO DEL CANCRO PROSTATICO ANDROGENO-INDIPENDENTE
- 3. Carcinoma della prostata • Più frequente causa di morte dopo i tumori del polmone e del colon. • Eziologia multifattoriale: fattori genetici, familiari, fattori ambientali, stile di vita, età e stato ormonale. • Tumore inizialmente androgeno dipendente, • Terapia standard: blocco androgenico. • L’eterogenità cellulare: selezione di cloni cellulari androgeno-indipendenti. • Nuovi protocolli terapeutici: terapie combinate, intervenendo sulla molteplicità dei cloni cellulari. • Analisi di meccanismi, che intervengono nella trasformazione e progressione neoplastica in maniera complementare o indipendente dall’azione androgenica.
- 4. Fattori di rischio del carcinoma della prostata • Avanzare dell’età; • Fattori ormonali: Studi nell’animale e nell’uomo indicano un ruolo dell’azione androgenica sbilanciata ( nella carcinogenesi prostatica; e ruolo sinergico di composti simil-estrogenici (EDC); • Fattori razziali: più frequente nella popolazione afro- africana e più bassa nelle popolazioni asiatiche (polimorfismo di AR e dietetici); • Fattori dietetici: sovrappeso come fattore di rischio, azione protettiva da alimenti ricchi di fitoestrogeni, vit D, licopeni, acido retinoico)
- 5. Secrezione ed azione degli androgeni
- 6. Schematic illustration of the location, exon structure and protein domain structure of the AR gene
- 7. Molecular events of androgen-AR action in a target cell, and the 5α-reductase action.
- 8. Meccanismo d’azione degli androgeni
- 9. Localizzazione di recettori androgenici nelle cellule prostatiche L’epitelio ghiandolare prostatico da cui origina il cancro della prostata ha tre tipi di cellule: • Cellule basali: Secernono i componenti della membrana basale, non sono androgeno-dipendenti, possono differenziare nelle cellule luminali; • Cellule luminali-secretorie: androgeno-dipendenti, vanno in apoptosi se deprivate da androgeni; • Cellule neuro-endocrine: androgeno-indipendenti. Alcune cellule stromali sono androgeno-responsive.
- 10. A graphic illustration of ligand-AR and ER cross-talk in the prostate cells.
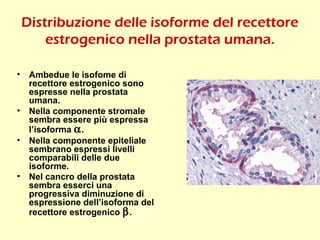
- 11. Distribuzione delle isoforme del recettore estrogenico nella prostata umana. • Ambedue le isofome di recettore estrogenico sono espresse nella prostata umana. • Nella componente stromale sembra essere più espressa l’isoforma α. • Nella componente epiteliale sembrano espressi livelli comparabili delle due isoforme. • Nel cancro della prostata sembra esserci una progressiva diminuzione di espressione dell’isoforma del recettore estrogenico β.
- 12. Progressiva diminuzione dell’espressione dell’isoforma beta del recettore estrogenico nella progressione di: •Ca. della mammella •Ca. ovarico •Ca. prostatico •Ca. colon
- 13. Cancro della prostata: Progressione verso la perdita della dipendenza androgenica: Alterazioni del signalling androgenico nel cancro della prostata
- 14. Pathway dell’ipersensibilità agli androgeni Aumentata sensibilità a concentrazioni di androgeni molto basse: le cellule tumorali non sono androgeno indipendenti, ma presentano una soglia più bassa per gli androgeni •amplificazione del gene del recettore androgenico •aumentata sensibilità del recettore androgenico alti livelli di espressione aumentata stabilità aumentata localizzazione nucleare •aumentato livello locale di androgeni aumentata attività 5 α reduttasica
- 15. Pathway “promiscuo” del recettore androgenico Acquisizione di cambiamenti genetici che portano ad una attivazione aberrante del recettore androgenico •Mutazioni del recettore androgenico mutazioni per sostituzione di base nel gene di AR che aumentano il numero di ligandi in grado di legare e attivare il recettore (estrogeni, progestinici, antiandrogeni) o ne variano l’affinità per coregolatori della trascrizione •Alterazione nell’espressione di coregolatori della trascrizione coattivatori (ARA70) corepressori
- 18. Pathway “fuori legge” Attivazione del recettore androgenico da meccanismi indipendenti dalla presenza del ligando •Attivazione da parte di fattori di crescita con recettori ad attività tirosin-chinasica (KGF, EGF, IGF). Necessario il LBD di AR •Attivazione da parte di recettori ad attività tirosin-chinasica (HER-2/neu) tramite MAPK. Indipendente dal LBD di AR. •Pathway di AKT (proteina chinasi B) ad attività antiapoptotica.
- 20. Pathway alternativo Modificazioni metaboliche che facilitano la proliferazione e inibiscono l’apoptosi delle cellule tumorali indipendentemente dalle vie di segnale del recettore androgenico Aumentata espressione del gene antiapoptotico BCL2
- 21. Meccanismi di sviluppo del cancro prostatico androgeno indipendente
- 22. Pathway delle cellule latenti Presenza di una sottopopolazione di cellule androgeno indipendenti prima dell’inizio della terapia antiandrogenica Le cellule staminali basali androgeno indipendenti presenti tra le .cellule basali della prostata trasformandosi danno origine al cancro prostatico. Possibilità di differenziare sia in cellule epiteliali che neuroendocrine I tumori prostatici contengono una miscela di cellule con diversa sensibilità agli androgeni come fattori di sopravvivenza e di crescita. La terapia antiandrogenica fornisce un vantaggio selettivo alle cellule androgeno indipendenti.
- 23. Selezione clonale di cellule androgeno indipendenti
- 25. Inter-relazioni del microambiente prostatico La progressione del cancro alla prostata è una cascata di eventi cellulari e molecolari che seguono una perturbazione iniziale in una complessa omeostasi bilanciata tra le cellule epiteliali, le cellule stromali, la matrice extracellulare, gli ormoni steroidei, il danno ossidativo e la presenza di sostanze cancerogene del microambiente prostatico. Lo studio dei meccanismi genetici e molecolari va quindi inquadrato nel complesso equilibrio dell’ambiente in cui si sviluppa il tumore
- 26. DIFFERENZIAMENTO DELL’EPITELIO PROSTATICO Cellule staminali prostatiche (AR- ) differenziano in • cellule intermedie “transit-amplifying” (AR- ) che successivamente maturano in cellule basali (AR- ) e cellule luminali secretorie (AR(AR++ )) ,, o in • Cellule Neuro-Endocrine (NE) differenziate quiescenti (AR- ), riconoscibili per marcatori specifici: cromogranina A, CD56, sinaptofisina, enolasi neurone-specifica, Sun Y et al. Am J Transl Res 2009
- 27. Cellule NE nella prostata normale COMPLESSA INTERAZIONE ESOCRINA/LUMINOCRINA, PARACRINA, NEUROCRINA, ENDOCRINA • Compartimento stromale (cellule nervose, fibroblasti, cellule endoteliali, cellule muscolari lisce, macrofagi etc); • Acini ghiandolari: epitelio secretorio luminale, epitelio basale; • Cellule NE presenti come cellule individuali disperse singolarmente nel compartimento epiteliale.
- 28. Prodotti di secrezione delle cellule NE • Serotonina • Calcitonina • Somatostatina • Catacalcina • Peptidi correlati con la cromogranina A • PTHrP (parathyroid hormone- related peptide) • Peptidi simili alla tireotropina e alla bombesina e gastrina • Neuropeptide Y • Vasoactive intestinal peptide (VIP) • aHCG • Colecistochinina • Survivina • VEGF • Fattori di crescita vari La secrezione include una varietà di molecole con funzione di ormoni, citochine, neuropeptidi, fattori di crescita e di sopravvivenza
- 29. Cellule NE sono presenti nel carcinoma della prostata. • Molto raramente i tumori prostatici sono composti prevalentemente da cellule NE (carcinomi neuroendocrini come il tumore a piccole cellule, o il tumore carcinoide). • Più comunemente, si ritrovano cellule NEPiù comunemente, si ritrovano cellule NE singole o in piccoli raggruppamenti nel contestosingole o in piccoli raggruppamenti nel contesto dell’adenocarcinoma prostatico convenzionale.dell’adenocarcinoma prostatico convenzionale.
- 30. Secrezione delle cellule NE tumorali. • Prodotti comuni al citotipo neuro-endocrino prostatico normale; • Prodotti ectopici: ACTH, ADH, encefaline, endorfine, progastrina, inteleuchina-8, ecc. • Produzione di isoenzimi 1 e 2 della 5alfa-riduttasi (possibilità che queste possano generare metaboliti steroidei più attivi, quali il DHT e il di-idrossi- progesterone, che a loro volta possono agire sulle cellule epiteliali tumorali vicine);
- 31. Effetti dei prodotti di secrezione delle cellule NE tumorali. • Bombesina:Bombesina: attiva il recettore dell’EGF, myc, fos;attiva il recettore dell’EGF, myc, fos; attiva NF-kB con aumento di Il-8 e VEGF;attiva NF-kB con aumento di Il-8 e VEGF; • Serotonina:Serotonina: agisce come fattore di crescita;agisce come fattore di crescita; • VEGF:VEGF: stimolo dell’angiogenesi;stimolo dell’angiogenesi; • Serotonina, calcitonina:Serotonina, calcitonina: amplificano l’azione di EGF, KGF,amplificano l’azione di EGF, KGF, IGF, VEGF;IGF, VEGF; • Survivina:Survivina: induce l’espressione del fattore anti-induce l’espressione del fattore anti- apoptotico bcl-2 ;apoptotico bcl-2 ; • Interleuchina-8:Interleuchina-8: stimola proliferazione androgeno-stimola proliferazione androgeno- indipendente del carcinoma e delle cellule NE;indipendente del carcinoma e delle cellule NE; • Somatostatina:Somatostatina: modulazione della secrezione delle cellulemodulazione della secrezione delle cellule NE; inibisce la proliferazione;NE; inibisce la proliferazione;
- 32. Le cellule NE influenzano le cellule cancerose circostanti Le cellule NE interagiscono con cellule secretorie epiteliali e con lo stroma, stimolando: • Proliferazione ed invasione, • Angiogenesi; • Resistenza ad apoptosi; • Androgeno-indipendenza (aumento dei fattori di crescita, azione di IL-8, resistenza all’apoptosi); • Pathway molecolari del differenziamento NE.
- 33. Il differenziamento NE è dipendente da vari stimoli Le cellule di PCa in coltura possono acquisire il fenotipo NE in seguito a vari trattamenti. In seguito a trattamento con epinefrina e forskolina che determinano l’aumento dei livelli intracellulari di cAMP, cellule LNCaP and PC-3 acquisiscono il fenotipo NE ed esprimono markers neuronali (Bang et al. 1994, Cox et al. 1999). Citochine, come interleuchina-6 (Qiu et al. 1998, Mori et al. 1999) ed interleuchina-1β (Diaz et al. 1998), ed alcuni fattori di crescita (Kim et al. 2002), possono indurre analoghi cambiamenti in cellule LNCaP in coltura In assenza di androgeni (medium di coltura deprivato di androgeni) cellule androgeno-dipendenti acquisiscono fenotipo NE (Zelivianski et al. 2001)
- 34. Yuan et al., 2006 In assenza di androgeni, cellule androgeno-sensibili di CaP esprimono alti livelli di recettore tirosin fosfatasi alfa (RTPα) che attivano c-Src portando a cascata di segnali con conseguente upregolazione di fattori di trascrizione specifici che inducono la trascrizioni di geni che portano all’acquisizine del fenotipo NE. Anche altri trattamenti con citochine, come Il-6, possono indurre il differenziamento nel fenotipo NE Pathway attivato della androgeno-deprivazione (Receptor protein tyrosine phosphatase α)
- 35. Deprivazione androgenica e fenotipo NE • L’acquisizione del fenotipo NE dipende dal microambiente tumorale: la deplezione androgenica è uno dei fattori che stimolano la via differenziativa, • Il trattamento androgeno-ablativo intermittente causa un minore differenziamento nel fenotipo NE rispetto a quello ininterrotto. Variation in chromogranin-A serum levels during intermittent versus continous androgen deprivation therapy for prostate adenocarcinoma. A Sciarra, S Monti, V Gentile, G Mariotti, A Cardi, G Voria, Lucera R and Di Silverio F. Prostate 2003: 55: 168-79
- 36. Microambiente citochinico e fenotipo NE Alcune citochine, come Interleuchina-6 , Interleuchina-1β, fattori di crescita ed altre molecole che fanno aumentare la concentrazione di AMPc intracellulare attivano cascate di segnali intracellulari che portano all’acquisizione del fenotipo NE. Importanza della risposta infiammatoria riparativa nel condizionare il microambiente tumorale, la progressione verso l’androgeno- dipendenza ed acquisizione del fenotipo NE
- 37. Up-Regulation of the Inflammatory-Reparative Phenotype in Human ProstateCarcinoma L Ravenna, P Sale, M Di Vito, A Russo, L Salvatori, M Tafani, E Mari, S Sentinelli, E Petrangeli, M Gallucci, F Di Silverio, and MA Russo Prostate 2009; 69 (11):1245-1255 Il fenotipo della risposta infiammatoria-riparativa è iperespresso nel cancro della prostata ed appare strettamente correlato con l’espressione dell’isoforma alfa del recettore estrogenico
- 38. L’attivazione di NF-κB favorisce la progressione neoplastica e l’acquisizione del fenotipo NE Il microambiente citochinico influenza il differenziamento in cellule NE
- 39. Ruolo del microambiente tumorale nella progressione neoplastica. Il microambiente tumorale determina la differenziazione in cellule NE che con la loro secrezione possono condizionare: • l’evoluzione delle altre cellule cancerose; • il comportamento delle cellule staminali stesse; • l’amplificazione di pathways alternativi (fattori di crescita, fattori anti-apoptotici, amplificazione della risposta infiammatoria da parte delle cellule tumorali); • ulteriore differenziamento in senso NE.
- 40. DIFFERENZIAMENTO NEUROENDOCRINO NEL CARCINOMA DELLA PROSTATA – ASPETTI PROGNOSTICI • Frequenza (10-100%) • Distribuzione sparsa nel contesto del tessuto tumorale epiteliale • Markers istochimici (Cromogranina A, NSE, CD56) • Differenziamento NE correlato con alto grado, alto stadio del tumore ed ormono-refrattarietà. • E’ stata descritta una prognosi peggiore per i pazienti con tumori con elevata presenza di cellule NE. • Dosaggio di marcatori plasmatici (Cromogranina A, NSE, ProGastrin-releasing Peptide)
- 41. Protocolli di terapia per il cancro della prostata.
- 42. Terapie combinate Somastatin analogues and estrogens in the treatment of androgen ablation refractory prostate adenocarcinoma. Sciarra A., Bosman C, Monti G, Gentile V, Gomez AM, Ciccariello M, Pastore A, Salvatori G, Fattore F and Di Silverio F. J Urol. 2004 Nov; 172:1775-83. The use of somatostatin analogues in combination therapy for D3 prostate cancer sus
- 43. Altre terapie: inibitori di NF-kB? Naturali • Curcumina • Flavonoidi • Genisteina • Resveratrolo Sintetici • Andographolide • Partenolide Inibitori del proteasoma • Disulfiram • Salinosporamide A • Bortezomib (PS-341) • etc
- 44. Multiterapie combinate? • Terapia ormonale (discontinua, estrogeni e SERMs….) ; • Inibitori di tirosin-chinasi; • Analoghi della somatostatina; • Inibitori di HIF-1a ed Nf-KB;