Tension 2006 2
- 2. Las superficies líquidas ¿Se deforman?
- 5. Experiencias en las que se manifiesta la tensión superficial
- 6. (B) (A) Anillo de alambre con un bucle flexible de hilo, introducido en una disolución de jabón: (A) antes y (B) después de perforar la película superficial del interior del bucle
- 7. EN EL ESQUEMA DE LA FIGURA AL ALAMBRE MOVIL DE PESO W 1 SE LE CUELGA UN CUERPO DE PESO W 2 . SIN EMBARGO SE COMPRUEBA QUE EL ALAMBRE NO SE CAE ¿CÓMO LO EXPLICA?
- 8. El alambre deslizante horizontal está en equilibrio bajo la acción de la fuerza superficial F dirigida hacia arriba y de la tracción hacia abajo, w 1 +w 2 . F = x 2 L L
- 9. La extracción de un anillo de longitud L, de una interfase, requiere que se efectúe una fuerza F opuesta a la fuerza de tensión superficial F . Este método se utiliza corrientemente para medir la tensión superficial. F F MÁX. = x perímetro
- 10. ¿Cuáles son las características de la Fuerza de Tensión Superficial?
- 11. Tangente a la superficie de la interfase Se opone a la fuerza deformante tendiendo siempre a disminuir el área de la interfase Se aplica en todo el perímetro de la superficie deformada Depende fundamentalmente, de la naturaleza de las superficies en contacto
- 12. La tensión superficial tiene como principal efecto el disminuir en lo posible la energía acumulada en las interfases . Por ejemplo, un líquido en ausencia de gravedad adopta la forma esférica, que es la que tiene menor relación área / volumen. Efecto de la tensión superficial
- 13. Definición del coeficiente de Tensión Superficial El coeficiente de tensión superficial ( ) es el trabajo (W) necesario para aumentar en una unidad el área de una superficie líquida.
- 14. El trabajo dW necesario para aumentar el área de una superficie líquida en la cantidad dA , es proporcional a ese incremento dW dA y la constante de proporcionalidad o trabajo por unidad de área, es el COEFICIENTE de TENSIÓN SUPERFICIAL dW = dA = dW/dA Unidades: ergio/cm 2 o dina/cm
- 15. El valor de γ depende de: la magnitud de las fuerzas intermoleculares en el seno del líquido. De esta forma, cuanto mayores sean las fuerzas de cohesión en el líquido mayor será su tensión superficial. la naturaleza de los medios en contacto
- 16. disminuye con la temperatura; el aumento de la agitación térmica redunda en una mayor energía de las moléculas que en mayor proporción tienen la posibilidad de contrarrestar las fuerzas intermoleculares de cohesión. disminuye con la la presión; especialmente cuando una de las interfases es gaseosa.
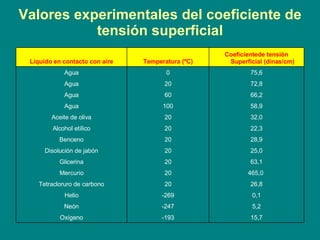
- 17. Valores experimentales del coeficiente de tensión superficial 5,2 -247 Neón 15,7 -193 Oxígeno 0,1 -269 Helio 26,8 20 Tetracloruro de carbono 465,0 20 Mercurio 63,1 20 Glicerina 25,0 20 Disolución de jabón 28,9 20 Benceno 22,3 20 Alcohol etílico 32,0 20 Aceite de oliva 58,9 100 Agua 66,2 60 Agua 72,8 20 Agua 75,6 0 Agua Coeficientede tensión Superficial (dinas/cm) Temperatura (ºC) Líquido en contacto con aire
- 19. Situación A: Fase sólida: Vidrio Fase gaseosa: Aire Fase líquida: Agua Situación B: Fase sólida: Vidrio Fase gaseosa: Aire Fase líquida: Mercurio ¿Cuáles son las diferencias entre estas dos situaciones? ¿Cómo se explican? A B Agua Mercurio
- 20. La superficie de un líquido, en la proximidad de una pared sólida, se curva diferente según sean las relaciones entre la tensión superficial sólido-vapor SV , sólido-líquido SL y líquido-vapor LV (b) (c) (a)
- 21. ¿Cuándo un líquido “MOJA” o “ NO MOJA” la superficie de un sólido?
- 22. ÁNGULO DE CONTACTO Es el ángulo “que contiene al líquido”. Se forma entre la superficie del sólido y la tangente a la interfase líquido-gas en el punto de contacto entre las tres fases (pasando por el líquido)
- 23. 140 Vidrio de sosa y cal Mercurio 107 Parafina Agua 29 30 29 33 Vidrio de sosa y cal Vidrio de plomo Pirex Cuarzo fundido Ioduro de metileno (CH 2 I 2 ) 5 6 45´ 20 30´ 21 Vidrio de sosa y cal Vidrio de plomo Pirex Cuarzo fundido -bromonaftaleno (C 10 H 7 Br) Ángulo de Contacto Pared Líquido ÁNGULOS DE CONTACTO
- 24. ¿Qué es una BURBUJA? ¿Qué es una POMPA? ¿cómo debe ser la presión interna respecto de la presión externa para que existan?
- 25. Sabemos que la Fuerza de Tensión superficial trata de disminuir la superficie de la interfase: t iende a colapsar la pompa o burbuja La Fuerza que se opone a la anterior e impide el colapso es la originada por la diferencia de presiones entre el interior y el exterior . Será necesario realizar trabajo para lograr un incremento del tamaño de la pompa P = F / A P = F. l / A . l P = dW / dV y dado que = dW / dA P / = dA /dV
- 26. LEY DE LAPLACE para gotas o burbujas Si V = 4/3 r 3 y A = 4 r 2 dV = 4 r 2 dr y dA = 8 r dr P = dA = 8 r dr = 2 dV 4 r 2 dr r P = 2 r
- 27. Ley de Laplace para superficies cilíndricas P = 4 r P = r Ley de Laplace para pompas de solución jabonosa P = P =
- 28. La presión en la pompa más grande es inicialmente menor, por lo tanto el aire fluye de la pequeña a la grande. El equilibrio se alcanza cuando las presiones internas se igualan. Entonces las curvaturas de las dos pompas deben ser iguales. Sólo se observará un casquete de la esfera de la derecha. ¿Qué sucede cuando se abre la válvula? A simple vista se observa que la pompa más grande crece y la más pequeña se achica aún más.
- 29. Las pompas siempre tratan de minimizar la superficie para un volumen dado
- 30. Apliquemos Laplace en estas dos situaciones: ¿Los sistemas están en equilibrio o evolucionarán de algún modo?
- 31. Ascenso y descenso capilar
- 32. R = radio del menisco P = R 2 P 5 P 1 P 4 =P 3 R 2 = h P 3 =P 4 P 3 P 4 P 1 =P 2 + R 2 P 2 + h=P 3 R 2 P 2 + =P 2 + h 1 2 3 4 5 3
- 33. Ley de Jurin 2 R = h R = radio del menisco r = radio del capilar R r cos = r / R 2 cos r = h
- 34. Apoyamos el objeto sobre un líquido Vemos que el sistema se encuentra en equilibrio. Por lo tanto: Tenemos un objeto y una interfase líquido gas Líquido Gas Objeto sujetado F P F La modificación de o de conducirá a un cambio del equilibrio original y, consecuentemente, a la generación de nuevos equilibrios caracterizados por otras relaciones P/ perim. Para un objeto dado P/ perim = k , por lo tanto el producto cos debe ser constante e igual a k si el equilibrio es vertical. perímetro cos P F y = P F cos = P
- 35. Compare la situación: 1 con 2 y 1 con 3 Qué cambió y qué no al pasar de 1 a 2 ó 3 ???
- 36. Barómetro de Fortín h 0 = h t – 0.123 t + c
- 37. Tabla de Kholraush Corrección por capilaridad Flecha f = h t – h` t h t h´ t
- 38. ¿Qué son los tensioactivos? : Son sustancias que al disolverse en un determinado líquido, inciden sobre la tensión superficial del mismo modificando el coeficiente de tensión superficial del sistema .
- 39. Hay tensioactivos que Aumentan el Disminuyen el
- 40. Dentro de ellos, los que disminuyen el coeficiente de tensión superficial (también denominados surfactantes) se utilizan en innumerables aplicaciones: productos de limpieza Industrias:Farmacéuticas , agro-alimenticias, cosméticas, metalúrgicas, textiles, petroleras, de pinturas y polímeros, etc. Aplicaciones de los tensioactivos :
- 41. Agentes tensioactivos surfactantes tienden a formar estructuras estables Región hidrofóbica Micela Las cabezas polares se orientan hacia el medio hidrofílico y las regiones no polares se ponen en contacto entre si. De este modo proveen un pequeño volumen hidrofóbico en un medio acuoso. Entre ellos los de cadena hidrofóbica no muy larga forman micelas .
- 42. Los de cadena hidrofóbica más larga como fosfolípidos o ácidos grasos tienden a formar liposomas que según el método de obtención pueden ser: Unilamelares Multilamelares Bicapas lipídicas que proveen un volumen hidrofílico encerrado en capas lipofílicas
- 43. Aplicaciones farmacéuticas En cosmética y farmacia se incorporan principios activos a liposomas los que debido a su estructura lipofílica favorecen la absorción El proceso de micelación juega un rol importante en la elaboración de preparaciones farmacéuticas, ya que el medio que proporcionan, facilita la disolución de otros compuestos
- 44. Micelas biológicas Durante la digestión se produce la micelación de los lípidos dietarios para favorecer su absorción Otras estructuras micelares son las lipoproteínas séricas fisiológicas (LDL, HDL, etc) Ácidos grasos Sales biliares triglicéridos fosfolípidos colesterol apoproteínas triglicéridos
- 45. Surfactante biológico en los pulmones
- 46. RESPIRACIÓN